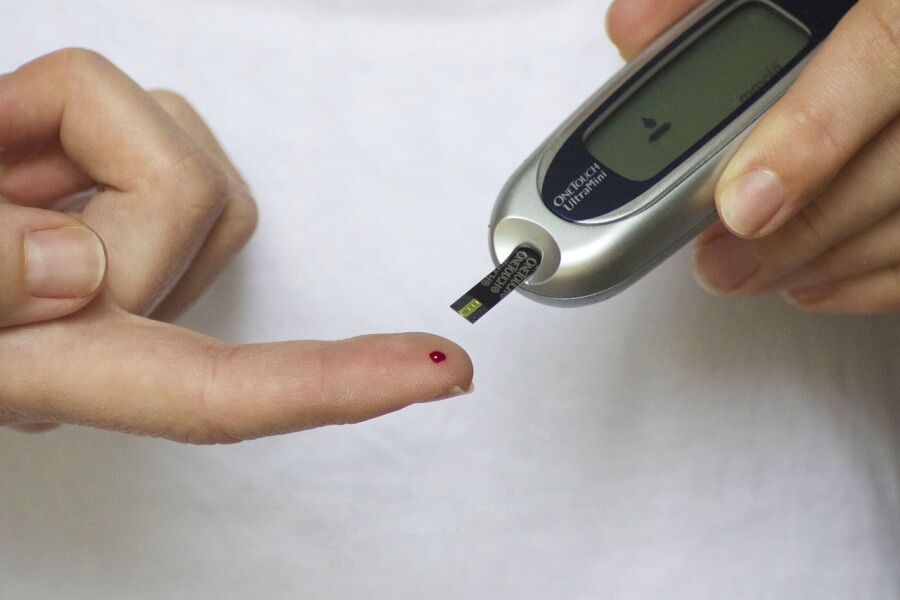
糖尿病が治りにくい原因
糖尿病は治りにくい疾病と言われていますが、これはなぜでしょうか?
日本の糖尿病患者のほとんどは2型糖尿病に分類されます。
2型糖尿病は生活習慣病の一つですが、生活習慣に加えて遺伝的要素が加わることで発症します。
この遺伝的要素の代表は「血糖値の上がりやすい体質」であり、糖尿病患者が治療によって血糖値を戻したとしても、血糖値の上がりやすい体質は変わりません。
また、糖尿病のリスク要因の一つである年齢も巻き戻すことは不可能です。
そのため、生活習慣を変えない限り、常に再発のリスク、中には「糖尿病には治る、治らないの概念はない」という意見も存在します。
とはいえ、生活習慣の改善によって、血糖値のコントロールによって、健康な人と変わらない状態に保つことは可能です。
糖尿病の治療は、多少の生活への制約はありますが、血糖値をコントロールすれば健康な状態を保つことができる、とも言えます。
この糖尿病の治療に幹細胞が大きな役割を果たすことが予想されていましたが、近年、実際にその治療方法が徐々に具体的になってきています。
1型糖尿病と2型糖尿病
糖尿病は発症原因によって、大きく分けると1型糖尿病を2型糖尿病に分類されます。
この2つの糖尿病は、特徴、治療方法が異なります。
1型糖尿病は、様々な原因によって膵臓のベータ細胞が破壊されて発症する疾病です。
膵臓のベータ細胞からはインスリンというペプチドホルモンを作って分泌しています。
インスリンは、血中のブドウ糖を肝臓、脂肪細胞、骨格筋細胞が取り込む時に誘導的な作用を持ち、炭水化物、タンパク質、脂肪の代謝を調節するホルモンです。
ベータ細胞が破壊されるとインスリンが分泌されなくなるため、1型糖尿病はインスリンが産生、分泌されなくなることが特徴です。
ベータ細胞が破壊されてしまう原因は正確にはわかっていませんが、いくつか予想されています。
予想されている原因の一つに免疫疾患があるとされています。
この免疫疾患は、自分の免疫システムが自分の細胞、つまりベータ細胞を攻撃して破壊するというメカニズムを持ちます。
最近になるまでは、1型糖尿病は「治らない」とされている疾病でした。
発症すると一生付き合っていかなければならない疾病だったわけです。
しかし近年になって1型糖尿病の治療方法が大きく進歩しており、再生医療、ランゲルハンス島移植などが研究されており、将来的には1型糖尿病は治る疾病になる可能性もゼロではありません。
一方で、2型糖尿病は日本の糖尿病患者の9割を占める疾病です。
2型糖尿病は、体質などの遺伝的要因、そして生活習慣が組み合わされることで発症する疾病です。
食事後、血中の糖濃度が上昇します。
この時、膵臓のベータ細胞からインスリンが分泌され、血中の糖濃度、つまり血糖値を低下させます。
食べ過ぎや運動不足などで、インスリンの分泌量が低下する、またはインスリンが効きにくい状態が続くと2型糖尿病が発症します。
2型糖尿病を発症した場合、初期の段階で生活習慣を改善できれば、血糖値を健康な人と同じレベルに戻すことは十分可能です。
しかし2型糖尿病が進行すると、健康なレベルに戻すことは困難になります。
そのため、2型糖尿病は初期段階での対応が重要になります。
滋賀医科大の糖尿病への挑戦
滋賀医科大学は、マーチャント・バンカーズ株式会社と共に、産学連携で糖尿病治療薬の開発推進を目的とした創薬ベンチャーとして、バイオジップコードを設立しました。
マーチャント・バンカーズ株式会社は、投融資のアレンジ、ホテルなどの運営を行う企業です。
もともとは西日本紡繊株式会社として繊維事業を行っていた会社です。
1960年代に西日本紡繊株式会社の経営を都築紡績株式会社が継承し、70年代に津島毛糸紡績株式会社と合併し、新日本紡績株式会社となりました。
2000年代に入り、国内繊維事業から撤退し、投融資のアレンジを主な事業とする会社になり現在に至ります。
滋賀医科大学では、再生医療開拓講座の小島秀人特別教授が中心となって、この産学連携事業を推し進めています。
滋賀医科大学は、小島特別教授を中心に2013年に生化学・分子生物学講座、再生・修復医学部門をスタートし、また2016年には医学部附属病院内に再生医療室を開設し、細胞調整室を作り、再生医療としての臨床基盤を整えてきました。
この研究グループは、「糖尿病を完治させる治療薬の開発」「細胞標的化技術の研究開発」を柱として、糖尿病分野では再生医療、とりわけ糖尿病などの難治性疾患の病因と考えられる造血幹細胞を特定するなど、独自に取り組んできた数々の研究を集大成し、これらを完治する治療薬の開発に取組んでいます。
そして共同で設立したバイオジップコード社は、糖尿病の治療法に関する2件の発明(異常幹細胞を標的とする糖尿病治療、幹細胞遊走剤を使用した糖尿病治療、ともに国内特許および国際特許の審査が進行中)の権利を同大学から譲り受けています。
滋賀医科大学はどんな研究を行ってきたか
バイオジップコードが譲り受けている特許の内容は、遺伝子治療により、ランゲルハンス島という臓器を丸ごと肝臓内で再生させ、インスリン依存型糖尿病を完治させることが理論的に可能であることを示したものです。
これまでに、ランゲルハンス島の分化を誘導する転写因子NeuroD遺伝子と、ベータ細胞の増殖因子ベータセルリンを、ヘルパー依存型アデノベクターに組み込み、糖尿病動物に投与した研究を進めています。
動物実験では、明らかな肝障害を示さず、血糖値は正常化、ブドウ糖負荷試験での血糖反応、インスリン反応ともに正常との差を認めないところまで改善させることに成功するなど、この研究は成果を生んでいます。
これらの研究成果は、糖尿病が完治しない原因となっている異常な幹細胞を、小島特別教授が発見したことにもとづくものです。
臨床への応用に向けて、その異常な幹細胞をターゲットにすることで、糖尿病の新たな診断薬の開発や、糖尿病を完治させる画期的な医薬品などを開発するきっかけとなる研究成果が産み出されました。
これらの研究成果を受けて、小島特別教授の研究グループでは独自の発見を治療方法に応用し、最近では糖尿病だけでなく、がん、自己免疫疾患などの難治性慢性疾患、多臓器不全ならびに従来の手術療法、そして薬物療法に治療抵抗性を示す疾病に対して既存薬の効果を拡大させる研究と新薬開発を進めています。
既存薬の効果拡大はリポジショニングと呼ばれ、糖尿病以外の疾患向けに治療薬として発売されている既存薬が、糖尿病を完治させることを目的としています。
リポジショニングによる開発は、新薬開発と比べて開発期間と開発コストを圧縮できるという利点があります。
既存薬は、すでにヒトでの安全性と体内動態が確認されていることから、臨床試験のうち、健康な成人を対象に安全性と体内動態を確認する第1相試験を行う必要がありません。
そのため、10年以上かかるとされる新薬の開発期間及び開発コストを大幅に削減できます。
具体的に進められている研究では、2型糖尿病だけでなく、主に自己免疫が原因に関わり、より完治が難しいとされる1型糖尿病にも適用が可能としています。
現在は治験計画の策定と、患者の治療プロトコール作成、そして実際の治験を目指す段階で、2027年までの販売開始を目指しています。
さらに新薬開発では、滋賀医科大学が開発を進めている細胞標的化ペプチドを用いた新たな薬物送達技術への応用や医療材料の開発も進めています。
この開発は、臨床治験の実施を目標としたもので、その延長線上に臨床応用を視野に入れて開発が進んでいます。
2022年時点で、特許登録や実用化の可能性が高いとされている滋賀医科大学の特許は9件が発表されています。
今後は糖尿病や再生医療など、長年の研究により集積してきた独自の技術やノウハウを活かし、医薬品や健康食品メーカー、研究機関などを対象に、アドバイザリー業務(学術・技術指導など)への取り組みも開始しています。
研究グループでは、糖尿病完治治療薬をはじめとする各プロジェクトの進捗については、同社のホームページでも随時掲載するとしています。