新型コロナウイルスとiPS細胞
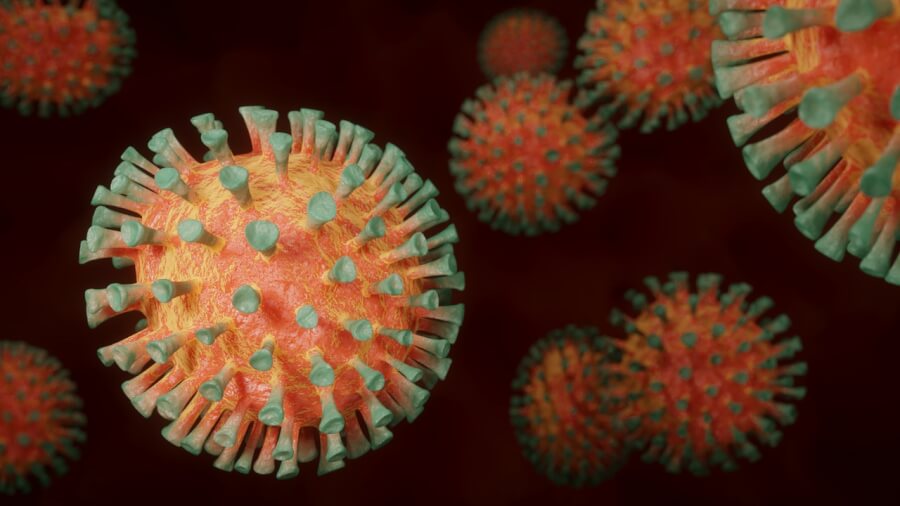
2019年末に発生した新型コロナウイルス感染症(COVID-19:Coronavirus disease 2019)は世界的に猛威を振るっています。
この感染症については、コロナウイルスの特徴、ワクチン、治療薬の開発が世界中で盛んに行われており、数年で関連論文、または開発品のプレススリリースが頻繁に発表される状況になっています。
このコロナウイルスの研究についての発表の中には、iPS細胞というキーワードがよく見られます。
iPS細胞といえば、再生医療が中心であり、新型の感染症の治療をどのように関わるかについては、なかなか一般の方には理解しづらい部分があります。
COVID-19の研究におけるiPS細胞の主な役割は、コロナウイルスの性質、動向を調べるための細胞の供給にあります。
コロナウイルスは主にヒトの呼吸器、気管、肺などに感染し、ヒトの細胞内に侵入して増殖します。
一般的にこういったウイルスは、偏性細胞内増殖、つまりは宿主の細胞内でしか増殖することができません。
そのためにヒトの細胞内に侵入するのですが、ヒト側から見れば細胞内に侵入させなければ増殖を阻止できるということになります。
こうしたメカニズムを研究するためには、実験室でヒトの気管、肺などの細胞にコロナウイルスを感染させて解析する必要があります。
意外と難しい、ヒト培養細胞とiPS細胞の出現によるブレイクスルー
人工的に培養し、研究などに使うことができる細胞、つまり培養細胞の存在を知っている人は意外と多いのですが、この培養細胞には欠点がある事はあまり知られていません。
ヒトの培養細胞のうち、がん化した細胞、例えば肝臓がんの細胞、肺がんの細胞などは比較的容易に培養実験に用いることができます。
しかし、がん化していない細胞、つまり健常細胞は培養がなかなか難しいという欠点をもっています。
がん化した細胞は、「無限増殖」といって、実験室内で増殖をし続けます。
体内においてもがん細胞の増殖力は健常細胞をはるかにこえており、その増殖速度こそが我々の健康に脅威を与えるものです。
そのため、人工的な培養ディッシュの中でもがん細胞は増え続けることができますが、健常細胞はそうはいきません。
健常細胞を人工的に培養しようとすると、細胞は数回程度の細胞分裂で増殖をしなくなってしまいます。
がん細胞は細胞分裂を無限にできる、または無限にできるからこそ問題となる疾患の細胞なのであって、本来は健常細胞のように細胞分裂の回数に制限がかけられています。
さらに、ヒトから気管、肺の細胞を採取するということも難易度が非常に高く、コロナウイルスを感染させる実験に十分な細胞をヒトから採取して確保するということは非常に難しいため、なかなかこうした研究を行うことができないのです。
しかし、iPS細胞の出現によって状況は大きく変わりました。
iPS細胞は多能性幹細胞のため、様々な細胞に分化させることができます。
つまり、肺の細胞でコロナウイルスの感染実験を行いたければ、iPS細胞を分化させてヒトの肺細胞を作成して感染実験を行うことができるのです。
肺細胞が不足した場合は、iPS細胞から分化させて肺細胞を供給すれば研究は継続できます。
この方法ですと、ヒトから採取した肺の健常細胞を準備する必要もありません。
iPS細胞は、再生医療だけでなく、こうした基礎的な医学研究の世界にも大きな変化を及ぼした細胞なのです。
コロナウイルスの特徴を解析する
iPS細胞から分化した細胞を用いて、東京大学の佐藤佳教授らは、新型コロナウイルスの変異株である「オミクロンBA. 5」の特徴を解析し、今回その結果を発表しました。
この研究は、東京大学だけでなく、北海道大学、宮崎大学、熊本大学、京都大学も参加し、大きな研究グループを構築して推進されました。
新型コロナウイルスのオミクロン株は、COVID-19の原因ウイルスのSARSコロナウイルス2(SARS-CoV-2)の変異株です。
2021年11月24日に南アフリカから世界保健機関(WHO)に報告されました。
このオミクロン株はSARSコロナウイルス2に比べると多数の変異を持っており、当初のワクチン標的としていたスパイクタンパク質の構造がこの変異によって影響されるために、伝染性、免疫の回避、ワクチンに対する耐性に対して懸念が生まれる結果となりました。
2021年末から2022年にかけて、オミクロン株はそれまでの主流であったデルタ株に取って代わり、世界の主流となりました。
オミクロン株内では、BA. 2、BA. 4、BA. 5という亜系統も出現しています。
感染者数の増加、拡大などの状況的には、デルタ株よりも感染性、増殖性が高いと考えられますが、実際にどれだけ早いのか、そもそも本当に増殖は早いのかどうかは、実験室内での解析が必要です。
東京大学を中心とした研究グループはこの解析を行い、オミクロン株のBA. 2に比べると、オミクロン株のBA. 5が増殖速度で1.4倍である事が明らかとなりました。
さらに、抗体に対する抵抗力が高く、ワクチン接種の効果がそれまでのコロナウイルス株と比べるとやや低いため、BA. 5株特異的なワクチンの開発必要性が出てきていることがわかっています。
どのような解析を行ったのか?
研究グループはまず、世界中のウイルスの全遺伝情報(全ゲノム情報)をベースとして、ヒト集団内でのオミクロン株の実効再生産数をコンピューターで推定しました。
その解析では、BA. 5のヒト集団での増殖速度はBA. 2の約1.4倍、そしてBA. 5とBA. 2は抗原性が異なるため、BA. 2で作られたワクチンは、BA. 5には聞きにくいことがわかりました。
そして、BA. 2に対するワクチンを3回摂取したときに得られる抗体に対しては、BA. 5は抵抗性を持っていることが明らかになっています。
さらに、ヒトiPS細胞を使ってヒトの肺細胞を構築し、コルナウイルス、オミクロン株BA. 5の感染実験を行いました。
- 2を感染させた場合と比較すると、BA. 5を肺細胞に感染させると増殖効率が高く、より早くウイルスが増殖していくことがわかりました。
ウイルスが細胞に感染するときには、ウイルスが宿主の細胞、コロナウイルスの場合はヒトの細胞と結合する必要があります。
この結合に大きな役割を果たすスパイクタンパク質に研究グループは着目しました。
- 2のスパイクタンパク質を持つウイルスを感染させたときよりも、BA. 5のスパイクタンパク質を持ったウイルスが感染したときの方が、動物感染実験に用いたハムスターの症状が悪化しています。
症状の悪化は、大きな体重減少と呼吸異常が中心で、この症状は生命に危険を及ぼすレベルでした。
2022年の8月時点で、COVID-19には全世界の6億人以上が感染し、わかっている範囲では600万人は死亡しています。
現在は、BA. 2からBA. 5に置き換わりつつある段階ですが、完全にBA. 5が主流となった場合、現在よりも死亡率が上がるのではないかと懸念されています。
コロナウイルスを撲滅することは可能か?
iPS細胞から分化させてコロナウイルスの感染実験を行うという手法は、この研究グループだけでなく世界中の研究グループで行われています。
たら・ればになりますが、もしiPS細胞がなかったら、新型コロナウイルスの特徴の解析はもっと遅れていたでしょう。
iPS細胞が分化誘導によってヒトの健常細胞を構築できたために、健常なヒトにコロナウイルスが感染すればどうなるのかという実験を研究室内で行うことができたわけです。
現在は、「コロナとの共存」などの言葉が出てきており、いずれインフルエンザと同様に季節性の流行が見られる疾患になるのではないかと予想されています。
インフルエンザは毎年、決まった季節に流行します。
つまり、インフルエンザウイルスを撲滅することは現時点でできてないということになります。
コロナウイルスも撲滅はなかなか難しいと考えられています。
感染メカニズム、注意すべき変異株、株に応じたワクチン開発などの研究によって、おそらく今後はヒトと新型コロナウイルスは共存するという状況になるでしょう。
COVID-19の流行によって、必要に迫られた人類はiPS細胞を使ってデータを集めて対策を練るという新しい研究方法を手に入れたと言ってもよく、今後はこの実験手法が頻繁に使われ、COVID-19の未知の部分を明らかにしていくのでしょう。