- 造血幹細胞は主に骨髄内に存在し、血球系細胞の生産を担っている
- 造血幹細胞の移植にはHLAの不一致から拒絶反応が起こる可能性があるものの効果の高い治療法である
- 造血幹細胞の治療には、ドナーの身体的負担や保存期間などの問題もある
ヒトの身体の中には血液が流れていますが、その血液のもととなるのが造血幹細胞です。
造血幹細胞は白血病、多発性骨髄腫、悪性リンパ腫などの「血液のがん」に対する治療に利用されますが、その治療に関する情報や課題をこの記事では解説します。
1. 血球系の細胞
血球系の細胞とは、赤血球、リンパ球、血小板などを指し、血液の中に存在して、血中で様々な役割を担っている細胞です。代表的な細胞を挙げますと、
- 白血球:リンパ球、好中球、好塩基球、好酸球、単球(マクロファージ)の5種類の細胞から構成されます。外部から侵入する細菌などの異物の排除が役割です。どの他にも、腫瘍細胞、役割を終えた細胞の排除にも働きます。
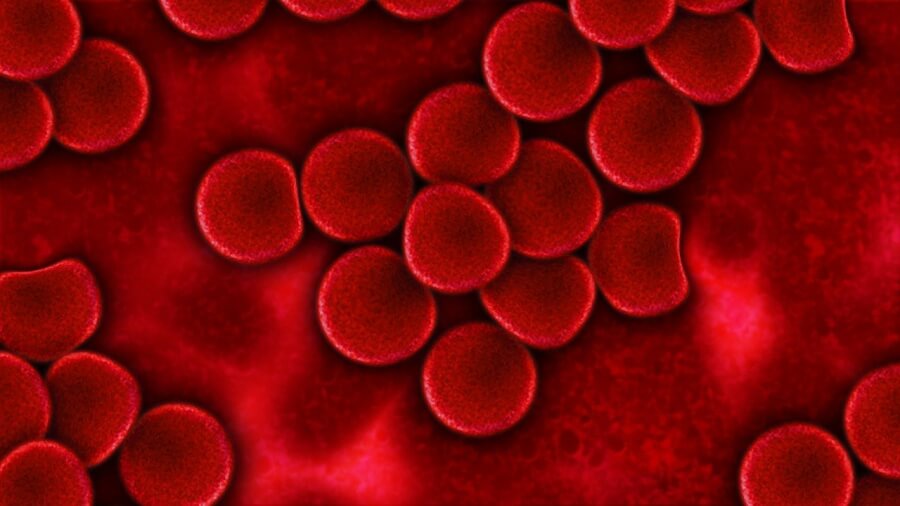
- 赤血球:酸素を運ぶ細胞です。また、二酸化炭素の排出のための運搬も行います。血液の体積のうち、40%から50%をこの赤血球が占めます。
- 血小板:血管の壁が損傷したときに、血小板凝集によって損傷部分に集まって傷口を塞ぐ役割を持ちます。止血に大きな役割を果たす細胞です。ここまでに挙げている白血球、赤血球と共に血球系に分類される細胞です。
これらの細胞には寿命があり、赤血球は約4ヶ月ほど、リンパ球の場合は数日のものもあれば10年以上のものと寿命に幅があります。好中球、血小板は寿命は短く、好中球では約24時間、血小板では3日ほどで寿命がきます。
これらの細胞は寿命によって次々と役割を終えて死んでいきます。それに対応して細胞を供給しないと、血中に必要な細胞がなくなってしまうため、造血組織からこれら血球系の細胞は常時供給されています。
ヒトの造血組織は、胸骨、肋骨、脊椎、骨盤などの体幹関連の骨に存在する、扁平骨、短骨の骨髄の中に存在します。ただしこれは成体のヒトの造血組織で、4ヶ月までの胎児の中では、卵黄嚢(らんおうのう)、肝臓、脾臓で造血します。このうち肝臓と脾臓は、成体になった後も血液疾患の時などに造血が見られる場合があります。
骨髄内には造血幹細胞、脂肪細胞、マクロファージ、間葉幹細胞が存在しており、この中の造血幹細胞が血球系細胞の生産に重要です。造血幹細胞が直接、または前駆細胞を経て各々の血球系細胞に分化し、血液中の細胞を供給しています。造血幹細胞は骨髄内の他の細胞と相互作用をしながら、血液中の様々な細胞に分化していきます。
2. 造血幹細胞の分化
造血幹細胞(HSC:Hematopoietic stem cell)は、血球芽細胞、骨髄幹細胞とも呼ばれ、ヒトでは主に骨髄に存在しています。
造血幹細胞は、白血球などの血液関連の細胞に分化する能力があり、1つの造血幹細胞が分裂後、2つの細胞がそれぞれ別種類の細胞になることができます。また、分裂後の細胞が幹細胞である、という分裂も可能です。これは幹細胞の特徴である自己複製であり、幹細胞が常に供給できるシステムになっています。
造血幹細胞は、血中成分である白血球に分類される、好中球、好酸球、好塩基球、リンパ球、単球、マクロファージ、その他の赤血球、血小板に分化します。他にも、免疫細胞として抗原提示の機能を持つ樹状細胞、炎症反応、免疫反応時に重要な役割を持つ顆粒細胞(別名:肥満細胞)にも分化します。つまりは、血液に関係するような細胞に分裂することが出来るということです。
3. 造血幹細胞の利用
例えば大量の放射線を浴びると、血液を造る機能(造血機能)に障害が生じます。この場合、別の個体の骨髄細胞を移植する事によって造血機能を回復させる事ができます。ただし、主要組織適合遺伝子複合体(MHC:Major histocompatibility complex、ヒトではHLA:Human Leukocyte Antigen)の一致している個体間の移植が望ましいとされています。臓器移植で拒絶反応が起きるという話を聞いたことがあると思いますが、それはこのHLAが一致しないからこそ起きる免疫の拒絶反応です。
このことは、骨髄細胞内に造血幹細胞が含まれている事の証明でもあります。骨髄細胞は1種類の細胞ではなく、造血幹細胞も含んで様々な細胞が存在します。現在は骨髄細胞群の中から造血幹細胞を分別し、純度の高い造血幹細胞を移植する事が可能となっています。造血幹細胞は1個の移植でも造血機能を回復させる事ができる場合があるので、この技術によって造血幹細胞の移植治療は飛躍的に進みました。
造血幹細胞移植によって治療される疾患は、白血病、多発性骨髄腫、悪性リンパ腫などの「血液のがん」に分類される疾患です。
また、がんの治療には放射線治療抗がん剤治療が用いられますが、これらの照射量、投与量を増やしていくと限界値に達してしまいます。この限界値は、骨髄抑制によって決められています。
骨髄抑制とは、白血球、好中球の減少によって起こる感染、感染による発熱、血小板減少による出血傾向、赤血球減少による貧血症状です。これらを作るシステムが照射量、投与量の増加によってダメージを受けて出現する副作用です。
しかし、がん治療時にはこの限界値をこえて照射、投与をする必要があると判断される場合があります。こうした場合、まずは放射線治療、抗がん剤治療を行って、ダメージを受けた造血機能の回復のために造血幹細胞を移植します。
臓器移植は、その臓器の機能などの回復が目的ですが、造血幹細胞の移植をする目的は、高い照射量での放射線治療、高容量の抗がん剤治療を可能とするためです。
ただし、造血機能の異常による疾患の場合は、患者の異常な造血機能をいったん放射線などで破壊し、正常な造血幹細胞を移植することによって造血機能を回復させるという治療方法もあります。
また、臓器移植では拒絶反応が起こりますが、造血幹細胞移植では臓器移植に伴う合併症(移植片対宿主病[GVHD:Graft versus host disease])がおこります。拒絶反応は、移植された側の免疫システムが移植した臓器つまりドナーの臓器に対して攻撃を加えますが、GVHDの場合は逆で、移植されたドナーの細胞、臓器のシステムが、移植される側を攻撃します。
しかし、造血幹細胞では免疫反応がおこらず、ドナー側の細胞、臓器からの攻撃が徐々に弱まります。そうなると、免疫抑制剤の投与量を徐々に減らしていく事ができます。造血幹細胞移植の場合、免疫抑制剤の投与は短期的にはGVHDの抑制で、長期的には免疫抑制剤の投与を減らしていく事が可能です。ただし、慢性GVHDが発症する場合もありますので、全てに適用できるわけではありません。
4. 造血幹細胞を使った治療の課題
造血幹細胞移植を伴う治療は、高容量の化学療法、放射線療法を伴いますので、患者の生活の質は低くなる傾向があります。造血幹細胞が直接の原因ではありませんが、重要な点です。
しかし、効果が見込める治療法ですので、これからも用いられ続けると思われます。現在、急性骨髄性白血病、多発性骨髄腫、悪性リンパ腫などに用いられていますが、造血幹細胞のソースを増やす事によって、必要な患者にどれだけ治療を提供できるのかがポイントになっています。
さらに、造血幹細胞を提供するドナーの身体的負担も問題の一つです。骨髄穿刺と呼ばれる骨髄の検査は造血幹細胞を採取するので、入院が必要です。また、全身麻酔下で行われますので、それらも抵抗がある人は多いかもしれません。
また、白血病の場合、造血幹細胞移植を受けても約30%の患者が、白血病を再発します。この再発防止の確率を減らす事は、造血幹細胞を用いた治療での課題になっています。
造血幹細胞自体が持つ課題についてですが、造血幹細胞を長期間保存し、機能を持ったままで移植する事はなかなか困難な事でした。しかし、最近になって、マウスの造血幹細胞を使って、長期保存の後も機能のロスなく移植できるような手法が開発されました。
造血幹細胞は、なるべく多くのタイプのHLAのヒトから採取したものをそろえておくと、必要なときにすぐに使う事ができます。しかし保存期間が長期になると機能が失われてしまうような状態では、なかなか多様なHLAのタイプの造血幹細胞を保有しておく事はできません。
この保存方法の発展によって、一度採取した造血幹細胞が長期にわたって保存できるようになれば、保存造血幹細胞のHLAの多様性が出てきますし、自身の健康なときの造血幹細胞を確保し、保存しておく事によって移植に対処する事もできます。今後、造血幹細胞の扱い方の技術の進歩によって、医療に使う幅が拡がると期待されています。