ALS(筋萎縮性側索硬化症)は、これまでに根治が難しいとされてきた進行性の神経変性疾患であり、既存の標準治療では「疾患の進行をわずかに遅らせる」ことがせいぜいでした。
しかし、近年「幹細胞」や「幹細胞上清液(conditioned medium, CM)」を用いた再生医療の試みが世界中で進み、「これまでの治療とは作用機序のまったく異なる、新たな可能性」として期待が高まっています。
本稿では、現在までの臨床および前臨床エビデンスを踏まえ、「幹細胞・上清液治療」の現状と限界、そしてなぜなお研究が継続されているのかを整理します。
ALS(筋萎縮性側索硬化症)とは?
筋萎縮性側索硬化症(ALS, Amyotrophic Lateral Sclerosis)は、脳および脊髄にある「運動ニューロン(上位運動ニューロン・下位運動ニューロン)」が徐々に変性・消失していく進行性の神経変性疾患です。
障害されるのは「身体を動かす神経」であり、筋肉そのものが一次的な原因で病気になるわけではありません。結果として、手足・舌・呼吸筋などが徐々に動かなくなり、筋力低下、筋萎縮、筋けいれん(ファシキュレーション)、こわばり(痙縮)などが出現します。
一方で、感覚(痛み・触覚)、視覚・聴覚、自律神経や内臓機能は比較的保たれるのが典型的です。
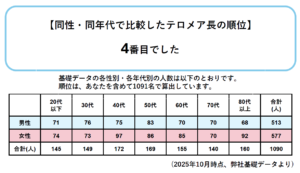
発症年齢のピークは概ね60〜70歳代で、男性にやや多いとされています(男性:女性 ≒ 1.2〜1.3:1)。
ALSの多くは原因不明の「散発性」ですが、全体の約5〜10%は遺伝性(家族性ALS)であり、SOD1 など特定の遺伝子変異が関与する例があります。
ALSは進行性・不可逆的で、現時点で根治療法は存在しません。診断後数年以内に呼吸筋の低下などにより生命予後が問題となることが多く、重篤な難病として各国の公的機関でも位置付けられています。
ALS(筋萎縮性側索硬化症)の基本的な治療法と効果
標準的に用いられている薬物療法
現時点で、各国のガイドラインや教科書レベルで「標準的」とされているのは、以下の薬物です。
リルゾール(Riluzole)
-
グルタミン酸作動性神経伝達を抑制し、神経細胞を保護すると考えられる薬剤です。
-
複数のランダム化比較試験のメタ解析により、生存期間を平均で数か月(おおよそ2〜3か月程度)延長することが示されています。
-
効果は「疾患を止める」のではなく、「進行をわずかに遅らせる」レベルとされています。
エダラボン(Edaravone)
-
強力なラジカルスカベンジャー(抗酸化薬)で、脳梗塞治療薬としても使用されてきた薬剤です。
-
ALS患者を対象とした臨床試験で、ALSFRS-R(ALS機能評価スケール)の低下速度を一定条件下でわずかに抑制したと報告されています。
-
ただし、効果は特定の条件(発症後1〜2年以内、呼吸機能がある程度保たれているなど)でのみ認められたとされ、総じて「限定的な効果」と評価されています。
トファーセン(Tofersen)
-
SOD1変異を有する家族性ALSに対するアンチセンスオリゴヌクレオチド(ASO)製剤です。
-
2023年に米国FDAが「加速承認」を行いましたが、根拠となったのは ALSFRS-R などの臨床指標ではなく、血中・髄液の NfL(neurofilament light chain)の低下というバイオマーカーの改善でした。
-
適応は SOD1 変異ALSに限られ、全てのALS患者に使える薬ではありません。
AMX0035(Relyvrio)
-
ナトリウムフェニル酪酸とタウルウルソデオキシコール酸の合剤で、ALSに対する神経保護効果が期待され、2022年に米国で一時承認されました。
-
しかし、その後実施された第3相試験で主要評価項目を満たせず有効性が否定的と判断され、2024年に米国・カナダで販売中止となっています。
まとめると
承認済み薬剤であっても、ALSに対する効果は「進行をわずかに遅くする」レベルであり、疾患を根本的に止めるものではありません。
支持療法・対症療法
薬物療法と同等かそれ以上に重要とされているのが、以下のような支持療法・対症療法です。
-
呼吸管理
-
非侵襲的陽圧換気(NIPPV)、必要に応じて気管切開下人工呼吸器。
-
呼吸筋の疲弊を軽減し、生命予後を延ばすことが示されています。
-
-
栄養管理・嚥下対策
-
嚥下障害に対して食形態の工夫、経管栄養(胃瘻など)を行うことで、誤嚥性肺炎や栄養不良のリスクを低減します。
-
-
リハビリテーション
-
理学療法・作業療法を通じて、残存機能を可能な限り維持し、拘縮や疼痛を予防します。
-
-
コミュニケーション支援
-
筋力低下で話すことが困難になっても、文字盤・タブレット・視線入力装置などを用いて意思疎通をサポートします。
-
これらはALSそのものを治すものではありませんが、生活の質(QOL)と生命予後に直接影響するため、各国ガイドラインで必須のケアとして位置付けられています。
幹細胞・幹細胞上清液治療との位置づけ
ここまでに述べた治療法が、現在「標準治療」として医学的エビデンスが認められている領域です。
一方で、幹細胞(間葉系幹細胞:MSC や神経幹細胞など)や、幹細胞上清液(conditioned medium, CM)を用いた治療は、現時点ではいずれも正式な標準治療には分類されておらず、「臨床試験段階の再生医療」という位置づけにとどまっています。
すなわち、研究としての可能性は検討され続けているものの、一般診療として有効性が確立した治療法とは見なされていません。
幹細胞治療のエビデンスの要点
幹細胞治療に関するエビデンスを俯瞰すると、2021年に発表された npj Regenerative Medicine のメタ解析では、ALSに対して行われた主にMSC(間葉系幹細胞)を用いた臨床試験13件、合計231例が統合的に解析されています。
この解析により、短期的な安全性については一定の情報が得られた一方で、ALSFRS-Rの低下速度といった有効性指標に関しては、「探索的な改善シグナルは存在するものの、結論を出すには不十分である」と評価されています。
すなわち、有効性を示唆する兆候は観察されているものの、それが偶然なのか、真の治療効果なのかを断定できるだけの統計学的な裏付けには到達していない、という位置づけです。
さらに、幹細胞治療の中でも最も大規模に検証されたものの一つが、NurOwn(自家骨髄由来MSCから神経栄養因子の分泌能を高めた細胞製剤)を用いたフェーズ3試験です。
この試験は189例を対象とした無作為化二重盲検プラセボ対照試験という、最も信頼性の高い臨床試験デザインで実施されました。
しかし、その結果、主要評価項目とされたALSFRS-Rレスポンダー割合において、NurOwn群とプラセボ群の間に統計学的に有意な差は認められず、試験は主要目的を達成できませんでした。
この結果を受けて、米国FDAの諮問委員会は「NurOwnには有効性を示す十分な証拠がない」として否定的な評価を下し、最終的にALSに対する治療薬としての承認には至っていません。
以上の流れを踏まえると、幹細胞治療は「まったく無意味」と断定できるほど研究が否定されたわけではないものの、少なくとも現時点では「標準治療として推奨できるだけの有効性は証明されていない」段階にあると整理するのが、科学的に妥当な評価となります。
一方で、現在の標準治療が「疾患の進行をわずかに遅らせる」ことしかできないという厳しい現実がある中で、幹細胞や幹細胞上清液は、これまでの治療とは作用機序そのものが異なるアプローチであり、神経保護や修復という観点から“理論上はまったく新しい可能性を持つ治療候補”として位置づけられています。
動物実験レベルでは生存延長や運動ニューロン保護といった効果も示されており、現時点ではまだ「仮説検証の途中段階」にすぎないものの、従来治療とは異なる次元の可能性を模索する研究対象であることは確かです。
ただし、これらの可能性が実際にヒトALS患者において「明確な治療効果」として証明されるかどうかは、今後の厳密に設計された大規模臨床試験の結果を待つ必要があります。
幹細胞上清液(conditioned medium)のエビデンス
幹細胞上清液(conditioned medium, CM)については、幹細胞そのもの以上に、ヒトALS患者を対象とした臨床研究の数が極めて限られています。
現時点で報告されているものとしては、日本の研究グループによる、乳歯由来歯髄幹細胞の上清液(SHED-CM)をALS患者15例に静脈内投与した単群試験がある程度です。
この試験では、治療に関連すると考えられる重篤な有害事象は報告されておらず、短期的な安全性については「許容範囲」と評価されています。
しかし一方で、この研究は対照群を設けていない単群試験であること、症例数が15例と極めて少ないこと、観察期間が短いことといった重大な制約を抱えており、これらの条件下では、治療による効果と自然経過による変化とを厳密に区別することができません。
そのため、この結果のみをもって「幹細胞上清液がALSに有効である」と科学的に結論づけることはできないのが実情です。
一方、前臨床研究、すなわち動物実験のレベルでは、ALSモデルマウスに対して脂肪由来MSCのconditioned medium(ASC-CM)を投与することで、生存期間の延長や運動ニューロンの保護効果が認められたとする報告が複数存在します。
これらの結果から、幹細胞上清液が神経保護作用を持つ可能性は、理論的には支持されていると言えます。
しかしながら、これらはあくまで動物モデルにおける結果であり、ヒトALS患者において同様の効果が再現されているとは現時点では言えません。
ALSの分野では、動物実験では有望な結果が得られたにもかかわらず、臨床試験で効果が否定された治療法が数多く存在しているのも事実です。
さらに重要な点として、現在市販あるいは自由診療で使用されている「幹細胞上清液」が、これら研究で用いられたASC-CMやSHED-CMと成分、濃度、製造工程、品質管理の点で同等であることを示す公的な検証データは、ほぼ存在していません。
このため、研究論文に基づく前臨床・初期臨床データを、そのまま市販製剤や自由診療の上清液治療に当てはめて評価することは、科学的には適切ではありません。
科学的に「言えること」
ALS(筋萎縮性側索硬化症)は進行性の神経変性疾患であり、現時点の医学では疾患そのものを根本的に治す根治療法は存在していません。
病状は時間とともに不可逆的に進行し、最終的には呼吸筋の麻痺などにより生命予後に大きく影響します。
現在、世界各国で承認されているリルゾールやエダラボンといった既存の治療薬は、ALSの進行速度をわずかに遅らせる効果が示されているものの、その効果は限定的と評価されています。
これらの薬剤はいずれも疾患の進行を完全に止めるものではなく、「進行を少し緩やかにする」「生存期間を平均で数か月程度延ばす」というレベルにとどまっています。
幹細胞治療については、骨髄や脂肪由来の間葉系幹細胞(MSC)を用いた臨床研究が世界各地で行われており、短期的な安全性については一定のデータが蓄積されつつあります。
しかしながら、これまでに実施された大規模な無作為化プラセボ対照試験において、ALSに対する有効性を明確に証明した研究は存在していません。
そのため、FDAなどの規制当局により承認されたALS向け幹細胞製剤は、現在に至るまで一つも存在していないのが現状です。
幹細胞上清液(conditioned medium, CM)については、ALS患者を対象とした臨床研究自体が極めて少なく、現時点ではごく少数の単群試験(対照群を設けない試験)にとどまっています。
これらの研究では安全性に大きな問題が報告されていない一方で、有効性や長期的な安全性を信頼性の高い形で示した大規模臨床試験はほぼ存在していないのが実情です。
科学的に「言えないこと」
現時点の医学的エビデンスに基づく限り、「幹細胞治療がALSの進行を確実に遅らせる、あるいは止める」と断定することはできません。
探索的な研究でわずかな改善傾向が示唆された例はあるものの、再現性が確認された決定的な証拠は存在していないため、治療効果を保証できる段階には至っていません。
同様に、「幹細胞上清液治療によってALSの症状が明確に改善し、寿命が延びる」と科学的に断言できるだけの根拠も、現時点では存在しません。
動物実験では神経保護や生存延長が示された研究もありますが、その結果がヒトのALS患者でも同様に再現されるかどうかは、臨床試験による検証が不十分です。
さらに、現在自由診療として提供されている幹細胞治療や幹細胞上清液治療が、学術論文や公的な臨床試験と同等の品質・有効性・安全性を備えていると保証できるだけの客観的データは存在していません。
製剤の由来、培養条件、成分、濃度、品質管理の方法は施設ごとに大きく異なる可能性があり、研究で用いられた製剤と同一であると科学的に確認できる情報が公開されていないケースがほとんどです。
まとめ
現時点において、「幹細胞治療」は「まったく無意味」と断定できるほど研究が否定されたわけではありません。
しかし、その効果を信頼できるかたちで「標準治療として推奨できる」と評価するための条件 ― すなわち、大規模かつ適切に設計された無作為化プラセボ対照試験による明確な有効性の立証 ― は、まだ満たされていません。
一方で、現在の標準治療が「進行のわずかな遅延」にとどまるという現実があるなかで、幹細胞や幹細胞上清液は、「神経保護」「神経修復」といった、従来の治療とはまったく異なる作用機序を持つ、新しいアプローチとして、理論上は“これまでにない次元の可能性”を秘めています。
動物実験では生存延長や運動ニューロンの保護といった成果も報告されており、ヒトにおける臨床応用が成功すれば、ALSの治療において画期的な進展となる可能性があります。
とはいえ、これらの可能性が「ヒトALS患者に対する明確な臨床効果」として証明されるかどうかは、今後の大規模かつ厳密に設計された臨床試験の結果を待つ必要があります。
そして、現状では「研究の途中段階」、すなわち「有力な治療候補」であるにとどまっていることを、冷静かつ明確に認識しておくべきです。
さいごに
現在、何らかの問題を抱えており、幹細胞もしくは幹細胞培養上清液を活用した治療を検討したいという方は、こちらのフォームからご相談ください。 ひやかしの質問や相談だと思われるものにつきましては、一切お返事しておりませんが、実際に悩みを抱えていらっしゃる方の真剣なご相談につきましては、すべて何らかの回答をさせていただいております。 ご相談いただく際には、できるだけ詳しい情報を記載していただくと、より適切な回答ができます。 年齢、性別、居住地、既往歴、現在抱えていらっしゃる問題はいつから悩まれているのか、これまでの治療やその効果、現在の状況など、できるだけ細かく書いていただければ、当機構の代表や関係ドクターの見解や当機構でお力になれる内容についてお伝えいたします。 ただし、「治験の紹介をしてほしい」というご相談をよくいただくのですが、残念ながらこれはできません。 治験というものは、製薬会社や医師が厚生労働省に届け出たうえで、新薬開発のために行う臨床試験で、国内で幹細胞に関わる治験も行われてはおりますが、その数はかなり少なく、極めて限られた範囲の疾病にしか適用されません。 治験に参加したいと言われる方は大勢いらっしゃるのですが、実際にはその中のほとんどの方が受けられないという現状があります。 当機構では、幹細胞やその培養上清液を、治験ではなく、すでに実際の治療に活用している国の機関の関係者や、病院、ドクターからの情報を直接得ながら、実際の治療につなげることが大事だと思っております。 特に、重篤な疾患等につきましては、治験を待っている余裕などないというケースがほとんどですので、状況に応じて、すぐに診察、治療を開始できるクリニック等におつなぎする方がよいと判断するケースが多々あります。 現在は他家幹細胞を使った治療は海外でしか受けられませんし、培養上清液を使った治療は国内で受けられるとは言っても保険が適用されないため自費診療になってしまいますが、それも含めて検討される場合は、遠慮なくご相談いただければと思います。 将来的には、日本国内において、他家幹細胞を使った治療ができるようになることや、幹細胞および培養上清液の治療が保険適用となるよう、当機構としては活動を推進していきたいと思っております。 お問い合わせ・お申し込みはこちら参考文献
- A randomized placebo-controlled phase 3 study of mesenchymal stem cells induced to secrete high levels of neurotrophic factors in amyotrophic lateral sclerosis
https://pubmed.ncbi.nlm.nih.gov/35182013/ - Looking backward to move forward: a meta-analysis of stem cell therapy in amyotrophic lateral sclerosis
https://www.nature.com/articles/s41536-021-00128-6 - The Safety and Efficacy of Stem Cell Therapy as an Emerging Therapy for ALS: A Systematic Review of Controlled Clinical Trials
https://www.frontiersin.org/articles/10.3389/fneur.2021.783122/full - Mesenchymal stem cell therapy in amyotrophic lateral sclerosis: a review
https://stemcellres.biomedcentral.com/articles/10.1186/s13287-023-03409-3 - Cell therapy in ALS: An update on preclinical and clinical studies
https://www.sciencedirect.com/science/article/abs/pii/S0361923023001446/