ヒトのiPS細胞から心筋系譜細胞作製、でもなぜ魚を使うのか?
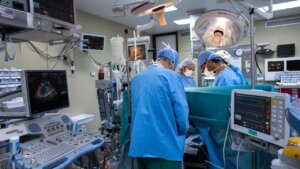
長岡技術科学大学の大沼清准教授らの研究チームは、ヒトのiPS細胞から作った心筋系譜細胞を魚に移植し、心臓に生着して動いていることを確認しました。
心筋系譜細胞は心筋細胞の前駆細胞であり、大沼准教授は「心疾患に対する効果的な薬剤や治療方法の開発への貢献が期待できる」と述べています。
さて、ここで疑問なのは、なぜ魚で生着を確認したのでしょうか?
これを理解するためには、大沼准教授の研究室で行われている研究の目的を知ることが必要です。
ヒトiPS細胞を分化させて様々な細胞を作る研究は、言い換えると「ヒトを作る技術の開発」と言えます。
倫理的な問題は当然ありますが、こういった研究は「ヒトiPS細胞の培養技術とマイクロ加工技術を組み合わせて、ヒトの胎児の身体作りを人工的に構築する技術の開発」です。
この技術によって、胎児に対する医薬品の安全性試験、人工子宮の技術、欠損してしまった組織、器官の再生が可能となります。
大沼准教授の研究室では、まず余分な成分を含まない培養液を使ってiPS細胞の研究を行っています。
細胞を人工的に培養するためには、培養液に「血清」を添加しなければなりません。
血清中には細胞の成長に必要な成分が含まれており、現在はウシの胎児などから採取した血清が使われています。
これらの成分は、薬剤などを加えた時に相互作用によって様々な影響を細胞に与えます。
つまり、実際の環境下でその細胞が応答する状況が作ることができません。
大沼研究室では、この血清を加えない無血清培地を使った研究で、毒性物質の作用メカニズムなどを調べていますが、実際に催奇形性を持つ薬剤であるサリドマイドで発現が変動する遺伝子を発見しています。
そして大沼研究室はiPS細胞から心筋細胞を作ろうとする研究をこれまで推し進めてきました。
細胞の多くは、自分に組み込まれた情報と、周囲の細胞が分泌するシグナルを使って将来どのような細胞になるかを決めます。
心筋細胞になるためには、細胞自身が抑制シグナルを分泌する「負のフィードバック」が重要であることを大沼研究室では明らかにしており、現在は心臓の形作り、つまりパターン形成のメカニズムを明らかにしようとしています。
さらに、生物の身体を形作る(発生生物学)メカニズムの研究のために、ヒトiPS細胞とマイクロパターン技術によって原腸形成の状態を人工的に再現し、細胞がどう移動しているのかについても研究しています。
胎児の奇形の原因となる催奇形性は、毒性物質によって細胞が正常な移動、パターン形成ができなくなることが原因の一つですが、この細胞の移動を認識することによって催奇形性を簡単に見分けるための技術をこの研究室では開発しています。
なぜ魚を使うのか?の答え
ヒトの心筋梗塞は、研究が盛んに行われている疾病の一つです。
ヒトの心臓は心筋梗塞を起こしてしまうと元通りには再生しません。
その再生を目指すためにiPS細胞を使った研究が多くの研究機関で行われています。
一方で、ゼブラフィッシュという魚は「心臓が再生する生物」の一つです。
つまりは、ヒトとゼブラフィッシュを比較すると、「なぜヒトの心臓(心筋細胞)はゼブラフィッシュのように再生しないのか?」が解明できます。
この研究で明らかにされた「ヒトとゼブラフィッシュの違い」は、ヒトの心筋細胞を再生するための研究に大きなヒントを与えます。
そしてプラナリアという生物も幹細胞の研究に大きなヒントを与えてくれる生物です。
プラナリアは魚類ではなく、扁形動物門に属する生物ですが、身体中にiPS細胞に似た細胞を持っている生物です。
中学、高校の教科書で、プラナリアを半分に切ると、切られた身体の破片からそれぞれプラナリアが発生する図を覚えている方もいらっしゃると思います。
つまり、切られたプラナリアは、体内のiPS細胞様の細胞を使って身体をそのまま再生します。
つまり、プラナリアの細胞を研究することは、そのままiPS細胞にも応用可能な知見を得られる可能性があるのです。
ゼブラフィッシュとは?
ゼブラフィッシュは、インド原産の5センチメートルほどの魚です。
日本ではシマヒメハヤ、シマハヤモドキと呼ばれており、コイ目コイ科に属しています。
金魚、コイ、オイカワに近縁の魚で、飼育、繁殖が容易、さらに流通価格も低価格で観賞魚としてもよく買われています。
生活環は3ヶ月から3ヶ月半、寿命は5年程度で雑食性です。
一組の雌雄が数百の卵を産むことが繁殖を容易にしている理由で、これも研究によく使われている理由です。
生物学、生命科学のモデル生物としては、マウス、ラットなどの哺乳類、ショウジョウバエなどの昆虫が知られていますが、ゼブラフィッシュもそれらに並んで汎用性のあるモデル生物です。
モデル生物としての有用性は、
- 飼育が容易であり、生物を飼育したことがない学生でも飼育が可能であること。
- 1日で数百個の卵を産むという多産であること。
- 世代時間が短く、生まれてから生殖を始めるまでは2ヶ月半から3ヶ月くらいである。
- 卵から孵化の過程では胚が透明なため、観察、そうさが容易であること。
これらが大きな理由になっています。
脊椎動物初の科学変異原ENUを用いた大規模変異スクリーニングはゼブラフィッシュで行われており、遺伝子機能の研究に欠かせない遺伝子導入、トランスジェニック作製をトランスポゾンを使って容易にでき、CRISPR/Cas9を使ったゲノム編集技術も確立されています。
マウス、ラットは生活環がそれほど短くなく、単価が高い、飼育するためには施設が必要です。
施設にはマウスなどの逃亡を防ぐ設備が必要なのですが、ゼブラフィッシュは水槽内から自力で逃げることはありません。
脊椎動物、という観点で見るとゼブラフィッシュはマウス・ラットと比べてランニングコストが安く済む実験動物です。
さらにゼブラフィッシュは遺伝子改変技術の確立によって実験発生生物学的な研究と遺伝子解析学を並行してできるモデル生物です。
このようなモデル生物は、Drosophila melanogasterとして世界で使われているキイロショウジョウバエにも当てはまります。
ショウジョウバエの場合、トランスポゾンを使った遺伝子改変が容易という点ではゼブラフィッシュと同様で、さらに生活環がゼブラフィッシュよりも短い10日程度です。
しかし、ショウジョウバエは脊椎動物ではないため、ヒトiPS細胞を使った研究では脊椎動物であるゼブラフィッシュの方が有利ですし、開放血管系であるショウジョウバエは心臓という臓器を持っていません(ヒト、ゼブラフィッシュは閉鎖血管系であり、管状の“血管”を持っています。そのため、その血管に血液を送り込むための“心臓”というシステムが必要です)。
研究チームの構成
この研究は、長岡技術科学大学の大沼研究室だけでなく、帝京大学、理化学研究所、そしてインドのアグハルカル研究所との共同で行われました。
帝京大学、理化学研究所(通称“理研”)はよく知られていますが、インドのアグハルカル研究所は日本国内ではあまり知られていません。
アグハルカル研究所は1946年にマハラシュトラ科学育成協会として設立されました。
インドは1947年8月にイギリスから独立しましたが、1946年はカルカッタの虐殺が起こるなど国内が独立運動の高まりと共に混乱していた時期です。
この時期に作られたというインド国内では伝統のある研究所です。
創設者はシャンカール・プルショッタム・アグハルカル(文献によってはアガルカール)教授で、1992年に創設者にちなんでアグハルカル研究所に解明されました。
1966年以来、インド科学技術省によって全面的に資金提供されている独立研究機関で、大学附属、附設研究所ではありません。
インドは、数学・情報などのレベルが高いとされてきましたが生命科学の分野にも積極的に進出しており、特にiPS細胞については新たなインドの産業となり得るとして多額の資金投下を行っています。