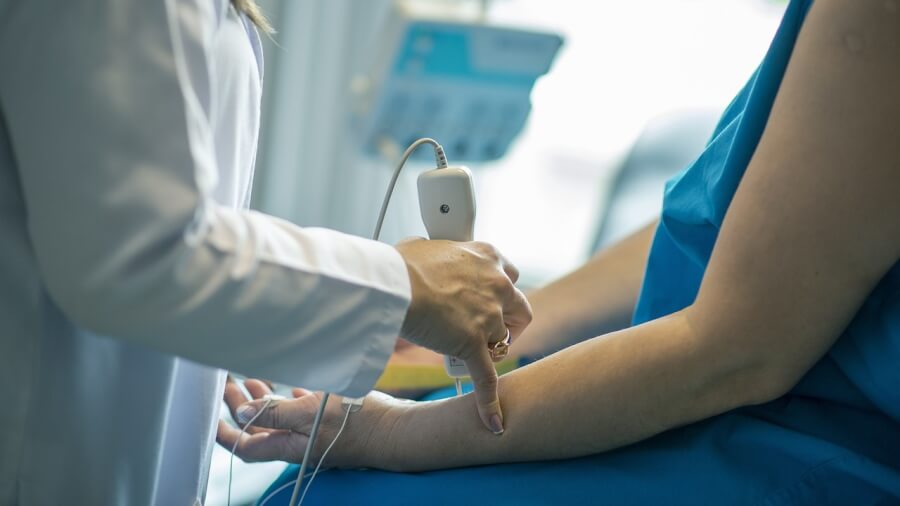
重症の糖尿病患者にiPS細胞による膵島細胞シート移植、京大病院が治験へ
京都大学附属病院はiPS細胞を用いて、膵臓の細胞が正常に機能しない1型糖尿病を治療する治験を開始。
対象となる患者は、血糖値を下げるインスリンが分泌されなくなり、膵島移植の必要性が出てきている20歳以上65歳未満の患者3人です。
計画の概略では、健康な人のiPS細胞から数センチ四方の膵島細胞シートを作成し、患者の腹部皮下に複数枚移植します。
その後、5年間経過を観察し、安全性などを確認することが今回の目的です。
糖尿病とは?
糖尿病は一般への認知度が高い疾患であり、患者数も多数確認されています。
糖尿病は、体内で血糖(血液中のブドウ糖)のレベルを適切に調整できなくなる疾患です。
これは、インスリンというホルモンの働きが不十分になったり、体がインスリンに対して抵抗性を持つようになったりすることで起こります。
糖尿病には大きく分けて2つの主なタイプがありますが、これらにはそれぞれ異なる原因と特徴があります。
まず、今回の治療の対象となる1型糖尿病です。
原因は、免疫系が誤って膵臓のインスリンを分泌する細胞(ベータ細胞)を攻撃し、破壊することで発生します。
そのため、体はほとんど、またはまったくインスリンを作れなくなります。
若い年齢で発症することが多く、インスリン治療が必須とされる疾患です。
そして2型糖尿病は、インスリン抵抗性が主な原因です。
これは、体がインスリンを適切に利用できなくなり、血糖値が上昇する状態です。
過体重や肥満、不適切な食生活、運動不足、遺伝的要因などがリスクファクターです。
中高年で発症することが多いですが、近年では若年層でも増加しています。
また、妊娠糖尿病と呼ばれる妊娠中に血糖値が高くなる状態もあります。
通常は出産後に回復しますが、将来的に2型糖尿病のリスクが高まることがあります。
糖尿病は完治しないものの、適切に管理することで合併症を予防し、健康的な生活を維持することが可能です。
糖尿病が適切に管理されないと、長期的にはさまざまな合併症を引き起こす可能性があります。これには、心血管疾患、腎臓病、神経障害、視力障害などが含まれます。
1型糖尿病とは?
今回の治療の対象となる1型糖尿病をもっと詳しく見てみましょう。
1型糖尿病は、他の糖尿病(特に2型糖尿病)と比べて次のような特徴があります:
・急速な発症: 症状が比較的短期間で現れ、進行が早いことが多くみられ、数週間から数か月で診断に至ることがあります。
・インスリン依存: ベータ細胞が破壊されるため、体内でインスリンをほとんど作れなくなり、インスリン注射が不可欠となります。
また、甲状性疾患などの他の自己免疫疾患と併発することもあります。
1型糖尿病の正確な原因はまだ完全には解明されていませんが、遺伝的要因と環境的要因が考えられています。
1型糖尿病はある程度遺伝的な素因があり、家族歴がリスク要因となることがある、これが遺伝的要因です。
ただし、遺伝だけでは説明できない部分も多く、ウイルス感染(例:コクサッキーウイルスなど)や食事、気候などの環境要因も、免疫系に影響を与え、1型糖尿病の発症を引き起こす可能性があるとされています。
1型糖尿病の治療には、インスリン療法が欠かせません。
インスリンを定期的に注射するか、インスリンポンプを使用することで、血糖値を管理します。
また、1型糖尿病は長期間にわたって管理を続ける必要があります。
適切に血糖値をコントロールできない場合、糖尿病性腎症、糖尿病性網膜症、糖尿病性神経障害、心血管疾患のような合併症が生じるリスクがあります:
1型糖尿病と膵島細胞の関係
1型糖尿病と膵島細胞(ランゲルハンス島)の関係は、1型糖尿病の発症メカニズムにおいて非常に重要な要素です。
膵島細胞は、膵臓の中に点在している細胞の集合体で、血糖値を調節するホルモンを分泌します。
膵島細胞には、特に1型糖尿病に関連する以下の3つの主要な細胞タイプがあります。
・ベータ細胞:ベータ細胞は、血糖値を下げるホルモンであるインスリンを分泌します。
食事をすると、血糖値が上昇し、それに応じてベータ細胞がインスリンを分泌します。
インスリンは、細胞がブドウ糖を取り込み、エネルギーとして利用するのを助けます。
1型糖尿病では、免疫系が自己免疫反応を引き起こし、誤ってこれらのベータ細胞を攻撃・破壊します。
この結果、インスリンをほとんど、または全く作ることができなくなります。これが1型糖尿病の主な病因です。
・アルファ細胞:アルファ細胞は、血糖値を上げるホルモンであるグルカゴンを分泌します。
グルカゴンは、血糖値が低下した際に肝臓からグルコースを放出させ、血糖値を上昇させる役割を果たします。
1型糖尿病での影響では、ベータ細胞が破壊されインスリンが不足すると、血糖値が不安定になります。
これに加えて、アルファ細胞からのグルカゴン分泌も制御されなくなり、血糖値がさらに上がる傾向が出ます。
・デルタ細胞:デルタ細胞は、ソマトスタチンというホルモンを分泌し、インスリンやグルカゴンの分泌を抑制する調整役を担います。
デルタ細胞自体は直接的に1型糖尿病に大きな影響を与えるわけではありませんが、全体的なホルモンバランスに関わっています。
1型糖尿病では、体の免疫系が誤って膵島のベータ細胞を「外敵」とみなし、攻撃を仕掛けます。
この自己免疫反応は、主にT細胞(免疫系の一種)が関与し、ベータ細胞を破壊します。
ベータ細胞が減少するとインスリンが作られなくなり、血糖値を下げることができなくなります。
1型糖尿病に対する治療として、膵島移植というアプローチが研究されています。これは、健康なドナーから採取した膵島細胞(特にベータ細胞)を患者の体内に移植し、インスリン分泌を回復させる方法です。
しかし、移植には免疫抑制剤が必要であり、また膵島細胞の提供も限られているため、現在は主に研究段階にあります。
1型糖尿病の根本的な治療法として、膵島細胞やベータ細胞の再生を目指した研究が進められています。
幹細胞治療や遺伝子治療の分野では、患者自身の細胞を使って新たなベータ細胞を作り出し、インスリンを分泌させるアプローチが模索されています。
iPS細胞と1型糖尿病治療の現在
iPS細胞を用いた1型糖尿病治療は、現在も研究が進んでいる段階ですが、非常に有望なアプローチとされています。
iPS細胞は、体のどんな細胞にも分化できる能力を持つため、膵島のベータ細胞を再生する可能性があると期待されています。
1型糖尿病の主な病因は、免疫系が誤って膵臓のベータ細胞を攻撃・破壊することにあります。
したがって、治療の目標は、これらのベータ細胞をiPS細胞によって再生し、再びインスリンを分泌できるようにすることです。
iPS細胞を用いた治療は、患者自身の細胞を使って膵島のベータ細胞に分化させ、それを体内に移植することで、インスリン分泌機能を回復させることを目指しています。
研究者たちは、iPS細胞をベータ細胞に分化させるプロセスの最適化に取り組んでいます。
この過程は非常に複雑で、多段階にわたる成長因子やシグナル伝達経路の制御が必要です。
そして作成したベータ細胞を患者の体内に移植する技術も並行して研究が進んでいます。
現状では、膵島移植の技術が応用されており、iPS細胞から作られたベータ細胞を患者に移植してインスリン分泌を再現する方法が模索されています。
ただし、ベータ細胞を免疫系から守る必要があるため、免疫抑制剤の使用や、細胞を包むバイオマテリアルを使った「カプセル化技術」などが試されています。
1型糖尿病の患者では、自己免疫反応がベータ細胞を攻撃するため、移植した新しいベータ細胞も同様に攻撃されるリスクがあります。
このため、免疫抑制剤の使用が課題となっています。
iPS細胞の研究では、免疫抑制剤なしでの治療を目指すため、免疫系を避ける方法や、患者の免疫反応をコントロールする技術(例:免疫寛容の誘導)が重要な研究分野となっています。
iPS細胞を用いた1型糖尿病治療は非常に有望ですが、いくつかの課題が残されています。
iPS細胞をベータ細胞に分化させるプロセスが十分に制御されないと、未分化の細胞が腫瘍を形成する可能性があり、臨床応用における安全性が最優先の課題となっています。
そして自己免疫反応が続く限り、新たに作られたベータ細胞が再び攻撃されるリスクがあります。
このため、免疫寛容を誘導する方法や、免疫系の反応を回避する方法が重要です。
最後に、 iPS細胞からベータ細胞を大量に作り出すための効率的なプロセスが必要です。
これが確立されれば、より多くの患者に治療が提供できるようになります。
iPS細胞を使った1型糖尿病治療は、まだ臨床応用には至っておらず、今回の治療試験の結果を待たなければなりません。
しかし、今後の研究が進展すれば、画期的な治療法として実用化される可能性が非常に高いです。