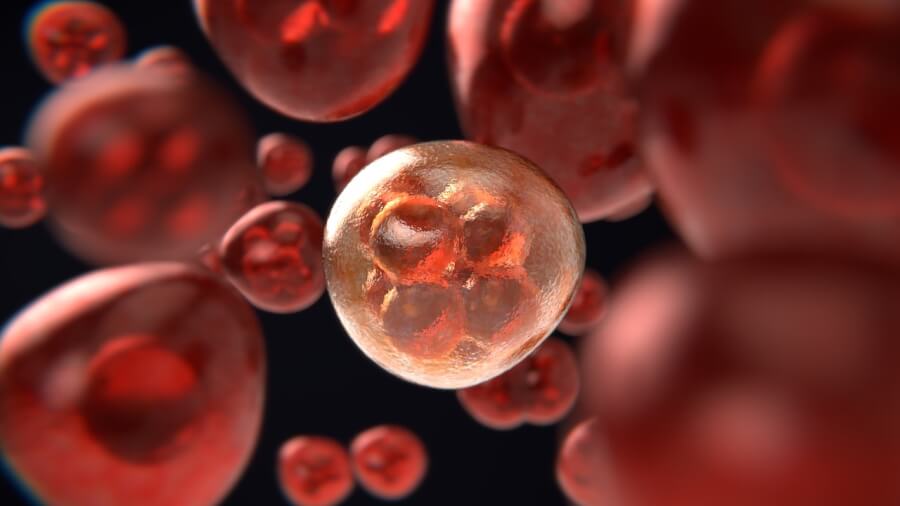
神経幹細胞とは
神経幹細胞は、自己複製能力と多分化能力を持った神経系の幹細胞です。
中枢神経系を構成する細胞は多種多様で、様々なタイプの細胞から構築されていますが、その多くが神経幹細胞から分化します。
特に胎児期には、神経幹細胞から多くの細胞が分化誘導されて脳を含む中枢神経系を構築します。
神経幹細胞は、脊髄損傷や脳梗塞に対する細胞移植治療としての応用が期待されています。
脊髄が損傷するケースは、交通事故、転倒事故、転落事故、またスポーツの競技中など様々なシチュエーションで起こります。
大きな力が外側から脊椎にかかった場合、骨折、間接部や靱帯が損傷することで脱臼してしまい、大きな損傷を受けます。
骨や靱帯が損傷するのみであれば、脊椎損傷と診断され、骨折や脱臼への治療で済みますが、骨折、脱臼が重いレベルで、その内部の脊髄までダメージが及んだ場合、手足の麻痺、感覚障害、排尿排便障害、呼吸障害、血圧調整障害などが起こります。
このような状態は脊髄損傷と呼ばれます。
細かく見ると、脊髄のダメージの程度によって生じる障害の程度も様々なことがわかります。
最も重症例は、動きも感覚も完全に消失するレベルですが、回復するケースも少なくありません。
受傷直後、早期に離床し、リハビリテーションを開始できるかどうかがカギとされています。
まず、受傷直後に専門的な集中治療を開始し、血圧、呼吸、体温などの全身状態をまずは安定させ、損傷した骨、靱帯を運動可能なレベル(あくまでリハビリテーションに耐えるレベル)に修復、または固定して、できるだけ安静時間を短くします。
安静時間を短くして積極的にリハビリテーションを行うことによって症状の改善が期待でき、医師のみならず、看護師、理学療法士、作業療法士などのチームが集学的な治療を行うことによって改善された例は少なくありません。
しかし現在、脊髄損傷によって10万人以上の患者が重度の麻痺などの大きな後遺症を抱え、車椅子生活や寝たきりの生活を余儀なくされています。
さらに、年間5000人以上が新たに脊髄を損傷しているのが実状です。
こういった症状の改善方法として、神経幹細胞を使った再生医療が注目されていますが、神経幹細胞の扱い方は難易度が高く、汎用性のある培養などの方法を確立が求められていました。
岐阜大学が行った研究の内容
岐阜大学応用生物科学部の中川寅教授、橋本美涼助教(以上、生物化学研究室)、千葉大学大学院医学研究院の粕谷善俊准教授、筑波大学生存ダイナミクス研究センターの深水昭吉教授らのグループは、タンパク質のアルギニンメチル化修飾が脳の大元である神経幹細胞の増殖や生存に必須であることを明らかにしました。
この研究のポイントは、
- アルギニンメチル化を触媒するための主な酵素である、PRMT1(Protein arginine methyltransferase 1 )の遺伝子発現がないと、神経幹細胞は増殖能力が低下し、細胞死が誘導される。
- PRMT1によるアルギニンメチル化修飾が神経幹細胞の増殖や生存に必須。
神経幹細胞は、脊髄損傷だけでなく脳梗塞の患者に対して移植治療することによって症状を改善することが期待されており、神経幹細胞の安定化に寄与する今回の研究は、神経幹細胞の培養技術に大きく役立つ治験であると考えられています。
この研究を理解するためには、3つの単語の意味を知る必要があります。
まず、PRMT1は、タンパク質アルギニンメチル基転移酵素1という酵素です。
アルギニン部位のメチル化は、細胞内の様々なタンパク質で見られる化学修飾の一つであり、タンパク質の局在や他のタンパク質との相互作用に影響を与えることで、細胞増殖や遺伝子発現制御といった多様な細胞機能を制御しています。
ニューロスフィアは、神経幹細胞を浮遊培養した際に形成される球状の3次元細胞塊です。
神経幹細胞自体の増殖や細胞同士の接着、凝集によって形成され、ニューロスフィアの細胞数やサイズを調べることにより細胞の増殖能や自己複製能を評価できます。
そしてアルギニンメチル化修飾は、タンパク質の修飾の一つであり、タンパク質の機能制御に関わる反応です。
哺乳類の主要な I 型アルギニンメチルトランスフェラーゼであるPRMT1は、ヒストンおよび非ヒストンタンパク質をメチル化し、転写、DNA 損傷応答、シグナル伝達などのさまざまな細胞機能を調節します。
研究の詳細
PRMT1は、ヒストンおよび非ヒストンタンパク質をメチル化し、転写、DNA 損傷応答、シグナル伝達などのさまざまな細胞機能を調節します。
PRMT1は神経幹細胞と胚の脳で高度に発現しており、PRMT1が初期の脳の発達に不可欠であることを示唆しています。
研究チームは、神経幹細胞活動における PRMT1 の役割を調べるために、神経幹細胞に特異的な PRMT1 が欠損したマウス胚の前脳から調製した 神経幹細胞を培養し、ニューロスフェアアッセイを実施しました。
PRMT1欠損神経幹細胞の一次神経球は小さく、数が減少していることが明らかになっています。
PRMT1が欠損している初代ニューロスフェアは、切断されたカスパーゼ-3のレベルが上昇しており、PRMT1欠損が細胞死を誘導したことを示唆しています。
さらに、p53 応答性の細胞死促進遺伝子は、PRMT1欠損神経幹細胞で発現上昇、活性上昇されており、PRMT1が存在しないと細胞死を誘導する経路が活性化することも明らかにされました。
これらは実験室内での人工的な培養環境での実験です
一方で、マウスを使った実験では、PRMT1が欠損している場合でも神経幹細胞は正常に増殖しました。
これは、神経幹細胞単体で培養して実験している人工培養の実験とは異なり、マウス脳内では周囲の異種細胞が何らかの形で神経幹細胞をサポートしているのではないかと研究宮ループは予想しています。
実験室内での人工培養実験の結果と、実際の動物脳内(マウス)の結果が異なるというやや複雑な結果ですが、この研究によって、
・神経幹細胞において、PRMT1は細胞の増殖や生存を制御すること。
・PRMT1欠損脳内では、脳の発達や恒常性維持のために、“神経幹細胞の生存を助けるような働きかけ”が起きていること。
この2つのポイントが明らかになりました。
今後どのように応用されるのか
この研究を足がかりとして、PRMT1の昨日とタンパク質の化学修飾メカニズムを明らかにすることによって、移植治療に用いる神経幹細胞の培養、調製方法の安定化、効率化に貢献することが期待されます。
神経幹細胞は先に述べたように、再生医療分野に置いて脊髄損傷、脳梗塞などの治療に有用であることが予想されており、この研究も含めて基礎的な知見の集積によって人工培養の安定化が望まれています。
iPS細胞から誘導した神経幹細胞を脳梗塞や脳・脊髄の損傷部位へ移植し機能的ニューロンを生み出すことで組織修復することが可能になれば、車椅子生活、寝たきり生活を余儀なくされる患者の数をでき敵に減少させることができることが予想されています。
今回、PRMT1が神経幹細胞の増殖、生存の維持に必須であることと、周辺細胞のサポートによってPRMT1に何かあっても生存が維持されることが明らかとなり、今後の人工培養技術は大きく進歩すると考えられます。
しかし、PRMT1が神経幹細胞内でアルギニンメチル化修飾を行うタンパク質がはっきりと同定されていません。
つまり、翻訳ご就職されるタンパク質そのものがいまだにわかっていないのです。
このタンパク質の特定が、この研究グループの次の目標とされていますが、どう対されたタンパク質の種類によっては、さらに安定的かつ効率的な人工培養技術の確立が見込めるかもしれません。