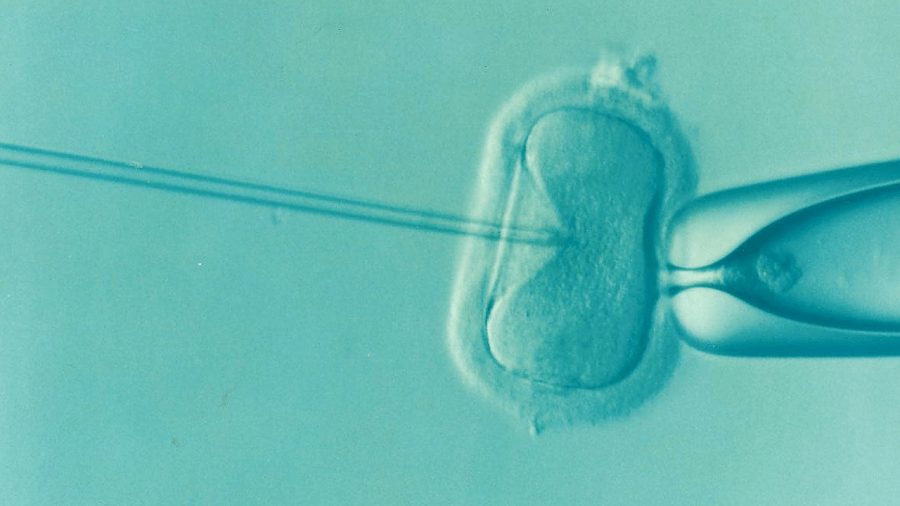
1. 卵胞とは?
生殖細胞である卵子は、ヒトの場合排卵されることによって受精が可能になります。
排卵するまでは、卵巣内で細胞に囲まれて成長します。
まず原始卵胞が全てのスタートです。
原始卵胞は一次卵母細胞という将来乱視になる元となる細胞を、顆粒膜細胞が取り囲んでいます。
この原始卵胞から一次卵胞、二次卵胞(前胞状卵胞)、成熟卵胞を介して排卵されます。
排卵のサイクルに合わせて、多くの卵胞が成長を開始しますが、通常排卵に至るのは1個の卵胞のみです。
卵胞は胎児からヒトの身体の中に存在しています。
胎児ですと約700万個と言われており、出産直後の赤ちゃんでは約200万個になります。
成長して思春期になると約20万から30万個と徐々に減っていきます。
30代後半では約25,000個、そして閉経をむかえる女性では1000個ほどになります。
多くの卵胞が成長を開始して、そのうちの1つが排卵されると先に述べましたが、つまりは生理周期1回につき、約1000個の卵胞がなくなっていくのです。
このメカニズムの中で何らかのトラブルが起きると、排卵されない、卵胞が成長しないなどの現象がおこり、妊娠しにくい、または不妊が起こることがあります。
そのため、不妊治療の開発では注目されている部分です。
生殖細胞について理解するためにはいくつかの用語を知る必要があります。
まず、卵原細胞です。
卵原細胞とは、胎児期のごく初期の卵巣に存在する生殖細胞で、減数分裂を開始する前の雌性生殖細胞です。
減数分裂とは、精子や卵子を形成するときに行われる細胞分裂の形態です。
細胞では染色体の数が分裂前の半分となり、減数分裂過程の組み換えによって新たな遺伝情報の組み合わせを持つ染色体が形成されます。
卵原細胞は胎児期に分化を開始し、卵母細胞という細胞になります。
卵母細胞は減数分裂中にある雌性生殖細胞ですが、この減数分裂が完了すると卵子になります。
2. 卵胞の人工培養に成功
京都大学高等学院、ヒト生物学高等研究拠点の斎藤通紀教授、水田賢助教らは、ヒトとカニクイザルを使って胎児の卵巣由来細胞から卵子の元となる原始卵胞を作成するための体外培養方法の開発に成功しました。
この研究グループは、iPS細胞から卵原細胞を構築することに成功していましたが、単元細胞をさらに分化させてヒトの卵胞を作るための体外培養方法は存在していませんでした。
研究チームは、ヒトのモデルとして、カニクイザル胎児の卵母細胞を使い、サル胎児の卵巣由来細胞の体外培養条件を解析しました。
その結果、約3ヶ月の培養期間を経て、サルの胎児の卵巣細胞から卵胞から誘導する培養技術を確立しました。
そしてカニクイザルで樹立した方法をヒト胎児の卵巣由来細胞に対して行ったところ、ヒトにおいても同様に卵胞の誘導に成功しました。
誘導した卵胞を解析すると、ヒト成人卵巣中の原始卵胞に近い性質を持っていることが明らかとなり、卵母細胞発生機構はカニクイザルとヒトで共通である事も明らかになりました。
この結果は、今後カニクイザルがこの領域におけるヒトのモデルとして有用である事を証明したことになります。
つまり、カニクイザルを研究することによって、ヒトの生殖細胞の発生メカニズムの解明、不妊症などの生殖細胞関連疾患の病因解明・治療開発を行うことができることになります。
3. 研究の詳細
今回の研究内容を詳しく見てみると、生殖細胞原因疾患の治療方法に貢献する結果が多数得られています。
まず、ヒトのモデル動物として、同じ霊長類に属するカニクイザルが有用である事が証明されました。
これまでカニクイザルはヒトのモデルとして多くの研究分野で用いられてきましたが、生殖細胞系列の研究においても有用である事がこれで証明されました。
研究では、まずサル胎児の卵巣由来細胞から卵胞を作成する技術の開発を目指し、8週齢胎児での生殖細胞が全て卵原細胞であった状態からスタートしました。
この状態で経過を観察すると、徐々に減数分裂を開始し、8週間から10週間で卵母細胞へと分化していきました。
そして18週齢になると、おおよそ半数の生殖細胞が原始卵胞を形成するという結果を得ることができました。
そして、8週齢胎児卵巣の細胞を使って、細胞凝集体、つまり卵巣を擬似的に再構成する処理を行いました。
この細胞凝集体をマウスの腎臓皮膜下に移植して12週間経過観察をすると、再構成された卵巣内に卵胞形成されていることが確認できました。
つまり、サルの胎児から構築した再構成卵巣は、適切な条件であればサルの体外(マウスの体内)でも卵母細胞への分化が進行し、卵胞形成が行われることが証明されました。
マウス体内で成功した後、次は完全に人工的な培養方法で誘導する条件を探るために検討のための培養を実施しましたが、マウスの卵胞培養で使われる気相液相境界面培養では上手くいかず、再構成卵巣はその形態を維持することができませんでした。
次に培養方法を浮遊培養方法に切り替え、液体培地などの比較検討を行いました。
その結果、長期間に渡ってサルの再構成卵巣を維持することに成功、12週間後には卵胞が誘導可能である事が明らかになりました。
組織学的な解析と、遺伝子発現パターンの解析によって、この体外培養環境でも、サルの再構成卵巣内で卵母細胞への分化が確認され、卵胞形成可能である事が証明されました。
4. ヒトの細胞でも成功
ここまではサルの8週齢胎児を使っていましたが、次のステップではヒト胎児の卵巣由来細胞を使って卵胞形成を試みています。
妊娠11週ヒト胎児からの卵巣由来細胞を使って同様の実験を行ったところ、14週間の培養期間の後にヒト再構成卵巣内に卵胞の形成が認められました。
確率としては、全生殖細胞中3 %で卵胞を形成しています。
さらに詳細を解析すると、人工的に誘導されたヒト卵胞は、生体と同等の卵母細胞分化過程を経ており、得られた卵母細胞はヒト成人の卵巣に存在する卵母細胞に近い遺伝子発現パターンを示していました。
これは世界初のヒトを含む霊長類胎児の単元細胞から卵胞を作り出す体外培養方法の確立となります。
さらに、この研究過程で得られたサル、ヒトの卵母細胞の解析によって、マウスとは異なる卵母細胞の発生機構が明らかになりました。
つまり、サル、ヒト特異的、霊長類特異的な卵母細胞の発生機構が明らかになりました。
サル、ヒト、マウスで共通の制御機構も発見されていることから、今後はモデル生物としてマウス、カニクイザルを使った場合の参考となる結果を研究グループは論文内で発表しています。
カニクイザルは、主に東南アジアに生息しているサルであり、ヒトやチンパンジー、オランウータンのようなヒト科の霊長類とは約2500万年から3000万年前に進化的に分離したとされています。
霊長類を使う際のモデル動物としてよく使われていますが、この研究ではカニクイザルを使ったことが功を奏した結果となりました。
5. 不妊治療の大きな進歩が期待できる結果
この研究によって、不妊治療に大きな進歩が起こると期待されています。
卵胞を人工的に誘導、培養が可能となったということは、卵母細胞、卵胞に問題を抱えた結果、妊娠しにくい、または妊娠できない場合の治療方法開発にメドが立ったということになります。
先進国で進行している少子化の原因は1つではなく、いくつかの原因が複合的に絡み合っていますが、その中には「子供が欲しいカップルに子供ができない」という不妊症も原因の一つとして認識されています。
一昔前までは、患者の不妊症の原因をはっきり特定できないこともありました。
診断方法、検査方法の進歩によって最近では不妊症の原因がかなり正確に特定されるようになりましたが、治療方法については開発がなかなか困難でした。
しかしiPS細胞の出現以来、再生医療によって不妊症が解消できる可能性が高まったことによって、治療方法の研究開発も盛んになってきています。
この研究を支援した国のプロジェクトのリストを見ると、国も期待していることが理解できます。
今後のこの研究の動向は注目に値するものとなるでしょう。