サルコイドーシスとは — 全身の臓器を脅かす肉芽腫の恐怖
サルコイドーシスは、全身のさまざまな臓器に「肉芽腫(にくげしゅ)」と呼ばれる炎症細胞の塊が多発する原因不明の疾患です。
免疫細胞の過剰な反応によって引き起こされると考えられており、厚生労働省の指定難病(指定難病84)に継続して定められています。
最新のデータである令和6年度末現在の調査によれば、特定医療費(指定難病)受給者証を所持している患者様は約1万6千人に上ります。
20〜30代の若年層と50〜60代の中高年層に発症のピークがあり、男女ともに罹患しますが、とくに女性は高齢になるほど発症が多くなる傾向にあります。
この病気の最も厄介な点は、肉芽腫が発生する場所が予測しづらいことです。
肺や肺門部(左右の肺の付け根)のリンパ節で発見されるケースが大多数を占めますが、眼、皮膚、心臓、神経、筋肉、さらには骨に至るまで、全身のあらゆる部位が標的となります。
症状は罹患した臓器によって全く異なり、長引く咳や息切れといった呼吸器症状だけでなく、霧がかったように見える視力低下、重篤な不整脈、さらには原因不明の極度な全身倦怠感など多岐にわたります。
経過観察のみで自然に寛解する患者様も多くいらっしゃる一方で、心臓や神経など生命維持に直結する臓器に病変が生じた場合や、肺の組織が硬くなる「線維化」が進行した場合には、命に関わることもあるため、早期発見と慎重な管理が欠かせない病気です。
現在の標準治療とその成果 — ステロイドがもたらす光と影
現在、サルコイドーシスの標準治療は、肉芽腫の形成とそれに伴う過剰な炎症を抑え、各臓器の機能低下を防ぐことを最大の目的として行われています。
最も中心となる治療法は、保険適用されている副腎皮質ステロイド(プレドニゾロンなど)の全身投与です。
心臓病変や神経病変、進行性の肺病変などがある重症例に対してこのステロイド内服治療が開始されると、多くの患者様において息切れや眼の強い炎症といった症状が速やかに鎮静化し、臓器の機能を守るという大きな成果を上げています。
眼や皮膚の限局的な病変に対しては、ステロイドの点眼薬や軟膏といった局所治療が選択されることもあります。
また、ステロイドの単独使用では十分な効果が得られない場合や、薬を減らすとすぐに症状が悪化してしまう患者様に対しては、メトトレキサートなどの免疫抑制剤が二次治療として使用されます。
この治療は、過剰に活発化した免疫反応を別の角度から抑え込むことで、副作用の強いステロイドの投与量を安全に減らしつつ、症状が落ち着いた状態(寛解)を長期的に維持することを目的としています。
これらは国内外のガイドラインでも推奨される治療であり、重症患者様の生命予後の改善と生活の質の向上に深く貢献しています。
既存治療の限界とアンメットニーズ — 難治化と副作用という高い壁
ステロイドや免疫抑制剤はサルコイドーシスの強力かつ有効な標準治療ですが、治療の長期化に伴って乗り越えなければならない深刻な課題も存在しています。
サルコイドーシスと診断された患者様のうち、約1〜2割は現在の標準治療を最大限に行っても炎症が十分に治まらない、あるいは進行が止められない「難治性」の経過をたどることが知られています。
また、いったん症状が治まる寛解状態に入ったとしても、ステロイドの投与量を少しずつ減らす過程で再び肉芽腫が悪化してしまう「ステロイド依存性」の状態に陥るケースも少なくありません。
さらに深刻な課題として、長期的な薬の副作用が挙げられます。
年単位でステロイドを内服し続けると、血糖値が上昇して糖尿病が誘発されたり、骨がもろくなる骨粗鬆症による圧迫骨折のリスクが高まったりします。
加えて、眼の緑内障や白内障、そして免疫力が低下することで重篤な感染症にかかりやすくなるなど、全身に多岐にわたる副作用が引き起こされます。
これらの副作用は患者様の日常生活を大きく制限し、治療の継続自体を困難にする要因となります。
そのため、全身の免疫を無差別に抑え込むのではなく、的を絞って炎症を鎮め、安全に寛解を維持できる新しい治療の選択肢が医療現場から強く求められています。
幹細胞治療が注目される理由 — mRNAレベルで書き換わる炎症のシナリオ
こうした既存治療の大きな壁を突破する次世代の治療法として、間葉系幹細胞(MSC)を用いた再生医療に熱い視線が注がれています。
MSCは、骨髄や脂肪組織などに存在し、体内の炎症を感知してそれを抑え込み、傷ついた組織を修復する機能に非常に優れた幹細胞です。
近年、この幹細胞がなぜサルコイドーシスに効果を示す可能性があるのか、その驚くべきメカメカニズムが「mRNA(メッセンジャーRNA:遺伝情報をタンパク質に翻訳するための設計図となる分子)」のレベルで解明されつつあります。
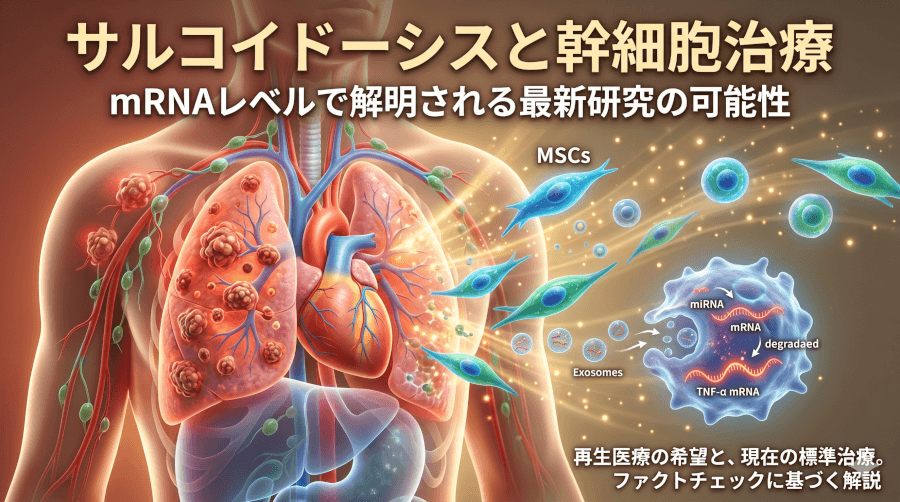
MSCが体内に投与され、炎症が起きている組織(肺など)に到達すると、「エクソソーム」と呼ばれるナノサイズのカプセルを周囲に一斉に放出します。
このエクソソームの中には、細胞の働きを制御するマイクロRNA(miRNA)という微小な核酸分子が豊富に詰め込まれています。
このmiRNAが、サルコイドーシスの肉芽腫形成の中心的な役割を担うマクロファージ(免疫細胞の一種)の内部に取り込まれると、炎症の元凶となるタンパク質(TNF-αなどの炎症性サイトカイン)を作り出すためのmRNAに直接結合します。
結合されたmRNAは分解されたり、タンパク質への翻訳が阻害されたりするため、結果として炎症物質が作られなくなります。
つまり幹細胞は、炎症の「設計図(mRNA)」の読み取りを強制的にストップさせることで、マクロファージの性質を攻撃的な状態から組織修復的な状態へと根本的に書き換えているのです。
この緻密なmRNA経路への介入が、ステロイドのような広範囲の副作用を回避しつつ、局所的な治療効果をもたらす鍵と考えられています。
国内外の研究・臨床試験の現在地 — マクロファージの働きを変える基礎研究
現在、サルコイドーシスに対する幹細胞治療は、世界中の主要な研究機関で精力的に研究が進められている段階にあります。
アメリカの国立衛生研究所(NIH)を中心とした2020年の画期的な研究報告では、サルコイドーシス患者様から実際に採取した肺のマクロファージに対し、骨髄由来のMSCを加えて培養する検証が行われました。
その結果、強い炎症を引き起こす「M1型マクロファージ」が、炎症を抑える「M2型マクロファージ」へと性質を大きく変化させ、主要な炎症性サイトカインであるTNF-αの産生量が劇的に減少することが確認されました。
これは、幹細胞が患者様自身の免疫細胞を直接「教育し直す」ことを証明した重要な基礎データです。
また、より実践的な海外の臨床研究においては、難治性の肺サルコイドーシスを患う患者様に対して、他家(健康な他人の)骨髄由来MSCを静脈から投与した症例報告が存在します。
このケースでは、幹細胞投与後に患者様の自覚する呼吸器症状が改善に向かい、血液検査における炎症反応の数値も速やかに低下したというポジティブな結果が示されています。
さらに過去を遡ると、アメリカの公的な臨床試験データベース(ClinicalTrials.gov)において、極めて重症の難治性サルコイドーシスに対する自家造血幹細胞移植の安全性・忍容性を評価する第I/II相試験(NCT00282438)も実施されています。
このように、細胞レベルの基礎研究から初期の臨床応用へと、幹細胞の可能性を示すデータが少しずつ、しかし着実に蓄積されているのが現在の現在地です。
期待される効果と残された課題 — 実用化に向けて乗り越えるべきハードル
幹細胞治療は、従来のステロイド治療や免疫抑制剤ではコントロールが難しかった「難治性」のサルコイドーシスに対して、炎症の根本的な鎮静化をもたらす画期的なアプローチになるとして大きな期待を集めています。
特に、エクソソームとmRNA経路の制御を通じたマクロファージの性質変化は、副作用を最小限に抑えつつ、長期間にわたって再燃を防ぎ、寛解を維持するための強力な武器となる可能性があります。
肺の線維化の進行を食い止め、心臓や神経といった重要臓器の機能を保つための新しい希望の光となり得るのです。
しかしながら、この治療を一般的な医療として実用化するためには、まだ乗り越えなければならない科学的なハードルがいくつも残されています。
最大の課題は、治療の標準化です。
現時点では、幹細胞治療がサルコイドーシスに対してどの程度の確率で有効性を示すのか、一度にどれくらいの細胞数を投与すべきか、また静脈点滴が良いのか気管支鏡を使った局所投与が良いのかについて、世界的な統一見解は定まっていません。
加えて、効果がどの程度の期間持続するのか、数年単位での長期的な安全性は確保されているのかといった疑問に答えるためには、さらに多くの患者様を対象とした厳格な臨床試験(第II相、第III相試験)を重ねていく必要があります。
未来展望 — 患者にとっての新たな希望の光
本記事で紹介した幹細胞治療の多くは現在研究段階にあり、国内外を問わずサルコイドーシスに対する標準治療として確立・承認されているわけではありません。
すべての患者さんに同様の効果が確認されているわけではないため、実際の治療選択にあたっては、必ず主治医にご相談ください。
安易に未承認の治療に飛びつくのではなく、現在の標準治療で得られる確実なメリットと、最新の研究動向が持つ可能性の双方を冷静に理解するこが、患者様自身の身を守る上で何よりも大切です。
それでも、再生医療の目覚ましい進化が、指定難病と闘う患者様にとって計り知れない希望であることは疑いようのない事実です。
幹細胞が放出する微小なエクソソームの働きや、mRNAという生命の設計図に対する分子レベルでの介入といった最先端の医学的アプローチは、かつては原因不明で治療が難しいと諦められていた疾患のメカニズムを、今まさに解き明かしつつあります。
研究者たちは日々、副作用の少ない安全な治療の実現に向けて歩みを進めています。
数年後、あるいは十数年後には、過剰な炎症を優しく正確に鎮める新たな治療法が、サルコイドーシスの克服に向けた選択肢として医療現場に届く日が来ると強く信じられています。
– 難病情報センター:https://www.nanbyou.or.jp/entry/110
– 厚生労働省:令和6年度 衛生行政報告例 特定医療費(指定難病)受給者証所持者数
– J Clin Med. 2020; 9(1): 278. (DOI: 10.3390/jcm9010278)
– Int J Med Sci Clin Res Stud. 2022. (DOI: 10.47191/ijmscrs/v2-i6-14)
– Front Immunol. 2021. (DOI: 10.3389/fimmu.2021.746996)
– ClinicalTrials.gov ID: NCT00282438
– プレドニゾロン錠 添付文書
サルコイドーシスの治療をご検討の方へ
サルコイドーシスは長期的な治療と管理が必要な病気であり、将来に不安を感じている患者様も多い病気です。
「今後の治療について情報を知りたい」「再生医療について知りたい」「治療の選択肢について相談したい」
そういった方に対して、治療の選択肢や情報を整理することは非常に重要です。
当機構では、再生医療に関する情報提供および相談対応を行っております。
ご相談をご希望の方は、下記お問い合わせフォームよりご連絡ください。