関節リウマチと免疫学研究の新展開
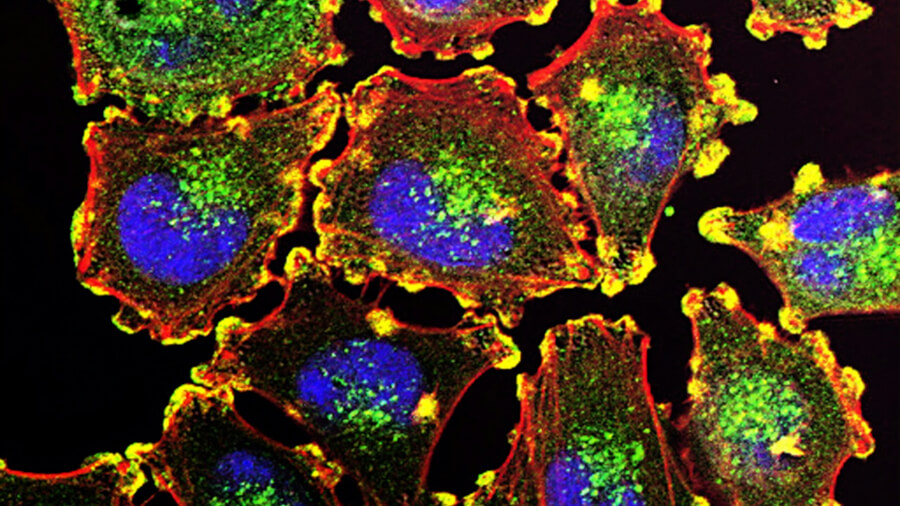
京都大学は8月5日、関節リウマチの病変部に存在するperipheral helper T細胞(Tph細胞)には、幹細胞に似た性質を持つ細胞(幹細胞様Tph細胞)と活性化した細胞(エフェクターTph細胞)の2種類があることを明らかにしたと発表しました。
関節リウマチ(RA)は、自己免疫応答によって関節に慢性的な炎症が引き起こされる代表的な自己免疫疾患です。国内外で数百万人規模の患者が存在し、日常生活や社会活動に大きな制約を与える疾患として知られています。
治療法の進歩により、近年では生物学的製剤やJAK阻害薬などが導入され、症状のコントロールや関節破壊の進行抑制に大きく貢献しています。
しかし一方で、薬剤に反応しない患者や再燃を繰り返す症例も少なくなく、より根本的な病態理解と新たな治療標的の探索が切望されてきました。
このような背景のもと、免疫学研究では病変局所に存在する免疫細胞の役割解明が重要視されています。
とりわけ、自己抗体産生を担うB細胞を活性化させるT細胞集団の同定は、病態進展メカニズムの解明に直結するテーマです。
その中で注目されているのが、Peripheral helper T細胞(Tph細胞)です。
Tph細胞は、リンパ節ではなく炎症組織の内部でB細胞を助ける特徴的なT細胞として近年報告され、関節リウマチをはじめとする自己免疫疾患の発症・維持に関わることが明らかになりつつあります。
幹細胞様Tph細胞という新しい概念
今回、京都大学の研究グループが報告したのは、このTph細胞の中に「幹細胞に似た性質を持つ細胞」と「活性化してエフェクター機能を発揮する細胞」の二つのサブタイプが存在するという新知見です。
前者は「幹細胞様Tph細胞」と呼ばれ、自己複製能や長期的な生存能力を持ち、病変組織の中で持続的に免疫応答を維持する可能性が示されました。
後者は「エフェクターTph細胞」としてB細胞を直接活性化し、抗体産生を誘導する役割を果たすと考えられています。
この発見は、病態の慢性化や再燃に関与する細胞集団の実態を明らかにするものであり、従来の「炎症を担う免疫細胞」という理解をさらに深化させる成果です。
特に「幹細胞様」という概念は、がんや造血研究の分野で重要視されてきましたが、自己免疫疾患の病変局所に適用されたのは新しい視点といえます。
今後、幹細胞様Tph細胞を標的とする治療戦略が開発されれば、従来薬では十分に制御できなかった患者層に対して、新しい治療選択肢を提供できる可能性があります。
このように本研究は、関節リウマチの病態解明のみならず、自己免疫疾患全体における免疫学研究の方向性を切り拓く重要な成果として注目されます。
関節リウマチの特徴と病態
関節リウマチ(Rheumatoid arthritis, RA)は、自己免疫の異常によって発症する代表的な慢性炎症性疾患です。
免疫系が誤って自己の関節組織を攻撃し、滑膜(関節を覆う膜)に炎症を引き起こすことが特徴です。
日本では人口の0.5〜1%、約60〜80万人が罹患しており、特に30〜50歳代の女性に多くみられます。
発症には遺伝要因と環境要因が関与しており、HLA-DR4など特定の遺伝子型に加え、喫煙や歯周病、感染症などが引き金になることが知られています。
活性化したT細胞やB細胞、マクロファージが炎症性サイトカイン(TNF-αやIL-6など)を放出し、滑膜が異常に増殖して「パンヌス」と呼ばれる組織が形成されます。
このパンヌスが軟骨や骨を侵食することで、関節破壊と変形が進行していきます。
臨床的には、手指や足趾の小関節に腫れや痛み、こわばりが現れるのが典型的で、30分以上続く朝のこわばりは診断の目安となります。
進行すると大関節に広がり、日常生活動作に支障をきたします。さらに肺や心血管、眼など関節外の合併症を伴うこともあり、全身性疾患としての側面も持ちます。
・診断と治療の進歩
診断には臨床症状に加え、血液検査(リウマトイド因子、抗CCP抗体)や画像検査(X線、MRI、超音波)が用いられます。
治療目標は「寛解」あるいは「低疾患活動性」の達成で、関節破壊を抑え生活の質を維持することです。
第一選択薬は抗リウマチ薬(DMARDs)で、その中でもメトトレキサートが基本となります。さらに、生物学的製剤(抗TNF抗体、抗IL-6受容体抗体など)やJAK阻害薬の導入により、従来はコントロール困難だった症例にも対応できるようになりました。
こうした分子標的治療は多くの患者に大きな恩恵をもたらしましたが、一部には薬剤抵抗性や副作用の問題も残っています。
そのため、新たな治療標的の探索と病態解明は現在も続けられており、今後のさらなる進展が期待されています。
Tph細胞とは何か
免疫系には多様なT細胞が存在し、それぞれが感染防御や免疫調節に関与しています。
その中で、Peripheral helper T細胞(Tph細胞)は比較的新しく報告されたサブセットであり、自己免疫疾患や慢性炎症の研究で注目されています。
従来から知られる「濾胞性ヘルパーT細胞(Tfh細胞)」はリンパ節の胚中心でB細胞を助ける働きを持ちますが、Tph細胞はリンパ節ではなく炎症組織や病変局所に存在する点が特徴です。
関節リウマチにおいては、炎症を起こした滑膜に集積し、B細胞を活性化して自己抗体の産生を促進することで病態を悪化させることが知られています。
Tph細胞は表面マーカーとしてPD-1を高発現する一方で、Tfh細胞の特徴的分子であるCXCR5を欠いています。
これによりリンパ節内ではなく、関節やその他の末梢組織にとどまり、B細胞と直接相互作用することが可能になります。
さらに、Tph細胞はIL-21やCXCL13といったサイトカインを産生し、B細胞の分化と抗体産生を強力に誘導する機能を備えています。
このように、自己免疫疾患の局所で「抗体産生を助ける存在」として機能する点で、病態の慢性化に大きな役割を果たしていると考えられています。
幹細胞様Tph細胞とエフェクターTph細胞
今回の研究で明らかになったのは、Tph細胞が一様な集団ではなく、性質の異なる二種類のサブタイプを含むことです。
第一は、幹細胞様Tph細胞です。この細胞は自己複製能をもち、長期間にわたり炎症組織内で生存する能力を持っています。
幹細胞のように「ストック」として存在することで、病変が慢性化した際にも持続的にエフェクター細胞へ分化できる供給源となり、疾患の再燃や長期化に関与すると考えられます。
つまり、病態の「根っこ」に潜む細胞として重要視され始めています。
一方で、エフェクターTph細胞は、すでに活性化されてB細胞と直接相互作用し、抗体産生を誘導する働きを持つ細胞群です。
彼らは短期的には炎症を増幅し、自己抗体や炎症性サイトカインの産生を介して組織破壊を加速します。
幹細胞様Tph細胞が病変局所で供給源として残り続ける一方、エフェクターTph細胞は実際に炎症を引き起こす「実働部隊」として機能している、と整理できます。
この二分化の理解は治療戦略に新たな方向性を与えます。
従来は炎症を抑えるためにエフェクター細胞やサイトカインを標的とした治療が中心でしたが、幹細胞様Tph細胞を標的にできれば、炎症を長期的に維持する根源的メカニズムを抑えられる可能性があります。
関節リウマチにおける難治例や再燃を繰り返す症例に対し、より根本的な治療効果が期待されるのです。
幹細胞様Tph細胞を標的とした新しい治療戦略
これまでの関節リウマチ治療は、炎症を引き起こすサイトカインや免疫細胞の働きを抑えることに主眼が置かれてきました。
代表例として、TNF阻害薬やIL-6阻害薬といった生物学的製剤、さらにJAK阻害薬などが挙げられます。
これらは多くの患者に有効で、疾患の進行抑制や関節破壊の予防に大きな効果を上げてきました。
しかし、一部の患者では薬剤に反応しない、あるいは治療中止後に病気が再燃するといった課題が残っています。
今回明らかになった「幹細胞様Tph細胞」の存在は、これまで見逃されてきた疾患の持続化メカニズムに光を当てるものです。
幹細胞様Tph細胞は病変組織内で長期的に残り続け、必要に応じてエフェクターTph細胞を供給する役割を担っています。
もしこの細胞を選択的に除去したり、その自己複製能を阻害する治療法が開発されれば、関節リウマチの「慢性化」と「再燃」の根源を断ち切ることが可能になるかもしれません。
これは、従来の対症療法的アプローチから、病態の根本原因に迫る治療への転換を意味します。
個別化医療と長期寛解への期待
幹細胞様Tph細胞の発見は、治療の個別化にも大きな影響を与える可能性があります。
今後、患者ごとに幹細胞様Tph細胞とエフェクターTph細胞の比率や活性を評価することで、病勢の進行度や再燃リスクを予測できるようになると期待されます。
これにより、現行治療で十分に効果が得られる患者と、新しい標的治療を必要とする患者を区別し、最適な薬剤選択を行う「精密医療」が実現するでしょう。
さらに、幹細胞様Tph細胞を制御する分子機構が明らかになれば、新たな分子標的薬や抗体医薬の開発につながります。
これにより、これまで難治とされてきた症例でも長期寛解、さらには薬剤を中止しても病気が再発しない「治癒に近い状態」の達成が可能になるかもしれません。
このように、今回の研究成果は関節リウマチ治療の未来像を大きく変える可能性を秘めています。
炎症を抑えるだけでなく、病気を持続させる“根源細胞”を標的にすることで、より持続的で根本的な治療戦略が現実味を帯びつつあります。